Гипоплазия костного мозга — что за болезнь
Вопрос №6 — Что такое гипоплазия костного мозга?
Артемьева Вероника из Нижнего Тагила спрашивает:
Что такое гипоплазия костного мозга, и какими симптомами сопровождается это заболевание?
Ответ эксперта:
Гипоплазия костного мозга – это состояние, при котором миелоидная ткань замещается жировой. Само понятие «гипоплазия» в переводе означает недостаточность формирования. При недостаточном формировании миелоидной ткани нарушается функция красного костного мозга, в результате чего значительно снижается выработка кровяных клеток – лейкоцитов, эритроцитов, тромбоцитов. Недостаточность костного мозга является одной из разновидностей панцитопении.
Причины развития
Существует две формы болезни:
Причиной развития наследственных форм являются следующие патологии:
- анемия Фанкони;
- врожденный дискератоз;
- анемия Даймонда-Блекфена;
- другие генетические заболевания.
Недостаточность выработки кровяных клеток может выступать в качестве самостоятельного заболевания при апластической анемии или развиваться на фоне следующих заболеваний:
- цирроза печени;
- хронического гепатита;
- злокачественных новообразований;
- различных аутоиммунных расстройств.
Проявления болезни
В организме больных людей объем крови гораздо ниже, чем у здоровых. В результате снижения количества тромбоцитов, у пациентов возникают спонтанные кровотечения. Опасность могут представлять любые порезы, травмы, приводящие к значительной потере крови. Кровоточивости подвержены слизистые оболочки и внутренние органы.
Недостаточность выработки лейкоцитов приводит к снижению иммунитета, способствующего возникновению частых инфекционных заболеваний.
Принципы лечения
Лечением данной патологии занимается врач-гематолог. Выбор способа терапии зависит от причины возникновения болезни. Апластическую анемию возможно устранить только путем пересадки костного мозга. Если не удается найти подходящего донора, больному показан прием препаратов, угнетающих иммунную систему (Циклоспорина А). Иммунодепрессивная терапия позволяет добиться успеха только при нетяжелых формах болезни.
Всем без исключения пациентам производят внутривенное введение тромбоцитарной и эритроцитарной массы. В целях предотвращения развития инфекционных и грибковых поражений больным назначается прием антибактериальных и противогрибковых препаратов.
Одной из причин недостаточного содержания кровяных клеток является повышение активности селезенки – гиперспленизм. Поэтому пациентам может быть проведена спленэктомия – операция, в ходе которой производят удаление селезенки.
Видео: Что такое трансплантация костного мозга
http://serdechka.ru/voprosy-otvety/gipoplaziya-kostnogo-mozga.html
Гипоплазия кроветворения
Гипоплазия кроветворения может развиться как синдром при туберкулезном процессе, но наряду с этим туберкулез может сочетаться и с истинной ГА [Любимова Л. С., Турбина Н. С. и др., 1968; Ulku В. et al., 1982].
В качестве такого примера можно привести одно наше наблюдение.
Больной Г. К., 52 лет, считает себя больным с ноября 1967 г., когда впервые появились быстрая утомляемость, кашель и периодическое повышение температуры до 40 °С. В январе 1968 г. были выявлены снижение содержания гемоглобина до 40 г/л, лейко- и тромбопения. Диагностирована гипопластическая анемия. Проведено лечение гемотрансфузиями с положительным эффектом. В апреле 1969 г. ухудшение: снижение уровня гемоглобина, снова появился кашель.
Анализ крови: Нb 68 г/л, эр. 2,8*10 12 /л, л. 2,8*10 9 /л, лимф. 96%. Миелограмма: бл. 4%, лимф. 68,6%. Геморрагий не было, несмотря на стойкую тромбоцитопению. Лечение гемотрансфузиями (всего 13), преднизолоном по 30 мг/сут (всего 2 г) на этот раз оказалось малоэффективным. При поступлении в ЦНИИГПК 01.08.69 г. состояние средней тяжести. Кожные покровы бледны. Подкожный жировой слой развит слабо, склеры слегка иктеричны. Периферические лимфатические узлы, печень и селезенка не увеличены. Билирубин 8,5 мкмоль/л свободный, прямая проба Кумбса положительная. Миелограмма от 12.08.69 г.: бл. 3,4%, лимф. 83,2%, красный росток 3,8%, пл. кл. 0,4%, встречаются скопления ретикулярных клеток, остеокласты, мегакариоциты (единичные в препарате), в редких полях зрения — свободно лежащие единичные тромбоциты.
В трепанате костного мозга на фоне общего рассасывания костной ткани видны участки оживления эндоста. Некоторые полости заполнены тканью типа грануляционной, среди которой видны отдельные фибробласты, гистиоциты, лимфоидные элементы. В других полостях строма крупноячеистого строения с отдельными элементами фиброретикулярной ткани. Элементы нормального гемопоэза почти отсутствуют.
Среди единичных сегментоядерных лейкоцитов, элементов красного ряда видны крупные темные клетки и клетки с небольшим круглым ядром, богатым хроматином, дифференцировать которые не представляется возможным. Заключение: подобная картина может наблюдаться при неоплазме, туберкулезе, бруцеллезе и других хронических инфекциях.
Таким образом, полученные данные указывали на угнетение кроветворения при каком-то другом заболевании. Поскольку у больного было периодическое повышение температуры (до 38 — 39 °С) и кашель, в первую очередь требовалось исключить туберкулез легких.
Однако кроме петрифицированных лимфатических узлов слева, свежих изменений в легких не выявлено. При рентгенологическом исследовании желудочно-кишечного тракта патологии не обнаружено. Многократные посевы крови были отрицательными.
Сканографическое исследование печени также не облегчило диагностику. Состояние больного постепенно ухудшалось, он стал худеть, лихорадка оставалась на высоких цифрах, признаки депрессии гемопоэза нарастали, развились правосторонняя нижнедолевая пневмония, некротический стоматит. При явлениях сердечной слабости больной умер.
На аутопсии: цирротический туберкулез легких с милиарным распространением процесса (легкие, селезенка, лимфатические узлы, печень), вторичный миелофиброз с угнетением кроветворения, нижнедолевая правосторонняя пневмония.
Данное наблюдение демонстрирует несколько важных клинических аспектов и в первую очередь трудности в установлении основного заболевания. Тем не менее высокая лихорадка при обнаружении петрифицированных очагов в лимфатических узлах корня левого легкого и гистологическая картина костного мозга должны были навести на мысль о целесообразности использования антитуберкулезных средств, хотя бы потому, что у больного применялся преднизолон.
Эта история болезни может служить примером и того, насколько глубоким бывает угнетение гемопоэза при другом заболевании.
«Депрессии кроветворения», О.К.Гаврилов,
Ф.Э.Файнштейн, Н.С.Турбина
http://www.serdechno.ru/depres/gipoplasticheskie/differenc/9696.html
Заболевания системы кроветворения. Гипопластическая и апластическая анемия
В основе заболевания лежит угнетение кроветворения, нарушение пролиферации элементов гемопоэза. Выделяют острую и подострую апластическую и гипопластическую анемию, хроническую гипопластическую анемию, гилопластическую анемию с гемолитическим компонентом.
Этиология. Определенную роль в возникновении заболевания играют эндогенные (эндокринные), экзогенные (химические, физические, токсико-аллергические, инфекционные) факторы.
Патогенез. В патогенезе важную (главную) роль играет нарушение процессов метаболизма в кроветворных клетках (понижение усвоения железа эритробластами костного мозга), синтеза гемоглобина.
Клиника и диагностика. Клиническая симптоматика острой апластической и гипопластической анемии, помимо выраженного малокровия, характеризуется кровоточивостью по типу тромбошпопенической пурпуры, анемией, лейкопенией, тромбоцитопенией.
Для апластической анемии характерно бурное нарастание анемизации со значительным снижением гемоглобина (30-60 г/л), эритроцитов (1-2х10,2/л), лейкоцитов (0,4-1,0х 109/л) (с лимфоцитозом 60-80%), тромбоцитов — до нуля. В разгаре заболевания нередко наблюдаются кровоизлияния в мозг, склеру и дно глаза.
При подострой гипопластической анемии геморрагические проявления выражены нерезко или отсутствуют. Гемограмма, миелограмма изменены несколько меньше. Течение хронической гипопластической анемии длительное с частыми обострениями. Эта форма анемии иногда сопровождается гемолитическим компонентом. При гипо- и апластических анемиях печень и селезенка, как правило, не увеличены. В костном мозге выявляются очаги гипоплазии кроветворения, выполненные жиром костномозговые полости и единичные участки кроветворения. Дифференциальный диагноз проводят с эритромиелозом.
Лечение. Показаны периодические переливания крови и ее компонентов: эритроцитной, лейкоцитной и тромбоцитной массы.
С гемостатической целью производят переливание плазмы, вводят эпсилонаминокапроновую кислоту, фибриноген, дицинон, проводят витаминотерапию (витамины группы В, никотиновая, фолиевая кислоты). В целях стимуляции гемопоэза назначают кортикостероидные гормоны (преднизолон и его аналоги в дозе 1-2 мг/кг), анаболические стероиды (нерабол, ретаболил и др.). Применяют трансплантацию костного мозга с тщательным серологическим подбором донора.
При прогрессировании анемии, геморрагическом синдроме, отсутствии эффекта от консервативного лечения, присоединении иммунного компонента и наличии антител к клеткам крови, а также при невозможности трансфузионной терапии показана спленэктомия. Во время и после оперативного вмешательства проводят переливание крови и ее компонентов, плазмы и др.
Послеоперационная летальность высока. Наиболее высокая летальность (37%) отмечается в первый год после операции, особенно у оперированных в фазе выраженного геморрагического криза (Л.С. Цепа, 1988).
Перейти к списку условных сокращений
Sosudinfo.com
Патологическое состояние, характеризующееся сниженным содержанием клеток крови и гемоглобина, называется анемией (народный вариант – малокровие). Уменьшенный показатель гемоглобина является основным необходимым признаком для постановки диагноза. Снижение эритроцитов при анемии может не наблюдаться и к определяющему критерию не относиться. Важно знать, что анемия не самостоятельное заболевание, а лишь проявление (симптом) основной патологии. При снижении уровня гемоглобина в крови должна проводиться тщательная диагностика, чтобы обнаружить причину симптома. Анемия развивается на фоне повышенной кровопотери, сниженного образования гемоглобина, усиленного разрушения клеток крови. По данным критериям ее подразделяют на следующие виды:
Общие понятия о гипопластической анемии
Гипопластической анемией является патологическое изменение картины крови вследствие подавления работы красного костного мозга. Проявляется это снижением выработки всех ростков крови (эритроцитарного, лейкоцитарного, тромбоцитарного) или только красного (уменьшение эритроцитов). История первого описания и появления данного заболевания начинается с 1888 года. В это время П. Эрлих выявил у девушки болезнь, проявляющуюся острым развитием кровоточивости, лихорадки, глубокой анемии и лейкопении. По результатам вскрытия и исследования костного мозга, признаков нарушения кроветворения выявлено не было. Анапластическая анемия как самостоятельное заболевание выделено Шоффаром в 1904 г. Позднее появилась апластичная анемия по типу Эрлиха с симптомами сепсиса, некроза, геморрагии и аплазии (отсутствие всех ростков кроветворения в костном мозге), проявляющаяся у молодых людей (18–20 лет). Основным контингентом, страдающим от данного заболевания, являются юные девушки и дети. В патогенезе развития выделяют несколько этапов. Сначала ткани, вследствие нехватки кислорода и питательных веществ, атрофируются и утрачивают свои функции. Далее жировая и соединительная ткани замещают погибшие клетки, что приводит к распространению патологического процесса. Прогрессирование заболевания происходит очень быстро и в случае отсутствия терапии может привести к смерти.

Классификация
В зависимости от происхождения гипопластическая анемия бывает:
- врожденной. Симптомы заболевания проявляются в раннем детстве и быстро прогрессируют. Причинами развития могут явиться генетические мутации ДНК у плода; наследственная предрасположенность (есть данные о подобной аномалии у кого-либо из родственников); нарушенное внутриутробное развитие (патологические изменения в системе кроветворения плода под воздействием неблагоприятного фактора). Исследования показали, что мальчики страдают врожденным апластическим синдромом в два раза чаще девочек;
- приобретенной. Данный вид гипопластической анемии характерен для любой возрастной группе.
Существуют идиопатическая (причина заболевания неизвестна) и миелотоксическая (предпосылкой является токсическое действие внешнего фактора) формы. К причинам, определяющим развитие миелотоксической формы анемии, относят:
- хроническую интоксикацию химическими веществами;
- лекарственные препараты с побочным действием на кроветворение (гормональные, транквилизаторы, цитостатики);
- облучение организма высокими дозами радиации (подвержены рентгенологи);
- заболевания эндокринной системы (могут осложниться гипопластической анемией);
- воздействие вирусов на клетки крови;
- на фоне туберкулеза и беременности также может развиваться гипопластическая анемия, но такие случаи встречаются в медицинской практике редко.
В зависимости от длительности течения заболевания выделяют:

В зависимости от массивности поражения костномозговых функций существуют патологии:
В зависимости от пораженных ростков крови выделяются:
По международной классификации болезней (мкб-10), анапластическая анемия имеет код D60 (эритробластопения – приобретенная красноклеточная аплазия), D61 (другие апластические анемии).
Выделяют три группы главных причин развития гипопластической анемии:

Механизм повреждения костного мозга заключается в том, что под действием вышеперечисленных причин происходит изменение хромосомного набора, вызывающее нарушенный синтез ДНК. Образование клеток крови тормозится и ткань красного костного мозга замещается жировой, которая не способна выполнять продуцирующую функцию. Общее состояние больного ухудшается, а картина крови представляется панцитопенией.
Основные симптомы патологии
Патогенез проявлений данной болезни объясняется неспособностью клеток крови (из-за низкого их содержания) выполнять свои функции. Таким образом, появление геморрагического синдрома обусловлено тромбоцитопенией и повреждением сосудистой стенки (недостаток серотонина и гипоксия приводит к повышению ее проницаемости).
К основным проявлениям геморрагического синдрома относят:
- частые беспричинные носовые кровотечения;
- появление кровоподтеков и синяков на коже при надавливании (пальцевая и манжеточная проба);
- кровотечение из десен;
- женщины часто жалуются на обильность и удлинение менструаций.
В случае затянувшегося патологического процесса или при массивном повреждении тромбоцитов могут развиваться такие осложнения, как профузное внутреннее кровотечение или инфаркт головного мозга с кровоизлиянием. В итоге это может привести к смерти больного.
Снижение иммунитета и сопротивляемости к инфекционным агентам связано с угнетением лейкоцитарного ростка. Гипопластическая анемия с иммунодефицитом представлена следующими симптомами:
Ребенок более подвержен таким изменениям, поскольку его организм находится на стадии активного роста и развития всех систем. Заболевание склонно к хронизации процесса с периодическими обострениями.

Уменьшенное образование эритроцитов приводит к развитию анемического симптомокомплекса:
В случае выявления остро протекающей тяжелой формы заболевания прогноз у такого пациента неблагоприятный: смерть наступает в течение 3 месяцев. Частой причиной летальности являются внутренние кровотечения или персистирующие инфекции, приводящие к сепсису.
Анализы крови и их расшифровка
Чтобы правильно поставить клинический диагноз, необходимо собрать анамнез, осмотреть пациента, провести пункцию костного мозга, исследовать кровь на признаки гипоплазии. Если при этом селезенка, лимфатические узлы и печень не увеличены, то можно выставить гипопластическую анемию.
Если это приобретенная форма заболевания, то анализ крови представлен:
- нормохромной (нет изменений цветового показателя), нормоцитарной (размеры эритроцитов в норме) анемией;
- содержание ретикулоцитов может быть сниженным или нормальным;
- лимфоцитопенией (уменьшена концентрация лимфоцитов), снижение происходит в большей степени за счет нейтрофилов;
- концентрация тромбоцитов снижена, что проявляется замедленным тромбообразованием и удлиненным временем кровотечения. При этом факторы свертывания в норме;
- происходит повышение общей железосвязывающей способности и сывороточного железа.
Если этиология заболевания имеет врожденный характер, то в крови выявляются следующие изменения:
- макроцитоз (увеличенный диаметр) эритроцитов;
- ретикулоцитопения (низкое содержание ретикулоцитарных клеток);
- показатель тромбоцитов и лейкоцитов в норме.
Апластическая анемия не поддается полному излечению. При выявлении на начальных этапах развития, правильной дифференциальной диагностике и своевременно начатом лечении можно добиться остановки прогрессирования патологии.
Лечение гипопластической анемии
Лечение заболевания проводят в зависимости от тяжести, степени выраженности проявлений и формы патологии. Выделяют следующие методы:
Консервативные
Оперативные
- при врожденной или аутоиммунной форме апластичного синдрома выполняют спленэктомию, что дает хороший результат;
- у лиц молодого возраста и в случае течения анапластического синдрома менее 3 месяцев производят пересадку костного мозга. Предварительно необходима диагностика донорского материала на НLA совместимость. До операции выполняется лучевая и иммуносупрессивная терапия.
Гипопластическая анемия является неизлечимой патологией, но при правильном лечении и выполнении рекомендаций доктора можно остановить прогрессирование заболевания и предупредить развитие осложнений. Выявив нарушенное кроветворение на начальных этапах, и проводя его правильное лечение, можно улучшить прогноз исхода событий.
http://sosudinfo.com/malokrovie/osobennosti-gipoplasticheskoj-anemii.html
Заболевания костного мозга: как лечить гипоплазию костного мозга?
При гипоплазии костного мозга, больной борется с сильнейшей анемией и угнетением костномозгового кроветворения. Как проявляется данное заболевание, и можно ли его вылечить?
Гипоплазия костного мозга — заболевание довольно редкое, и проявляется оно преимущественно у тех молодых людей, что не достигли по возрасту сорока лет. Какие симптомы при гипоплазии костного мозга встречаются, и может ли заболевание довести до летального исхода?
Как проявляется гипоплазия
Гипоплазия костного мозга — весьма опасное заболевание, и проявляется оно постепенно. Больные начинают жаловаться на одышку, постоянную усталость, шум в ушах и в боли в голове. Если на первые симптомы не обращать внимания, постепенно появятся небольшие подкожные кровоизлияния, а при развитии болезни человек начнет страдать из-за повышенной температуры и постоянной слабости.
Степень проявления тех или иных симптомов напрямую зависит от степени угнетения костномозгового кровопотока. Само заболевание сначала никак не проявляет себя, а болезненные признаки возникают уже на поздних этапах гипоплазии.
Геморрагические осложнения также наблюдаются на поздних этапах развития заболевания. К тому же, в стенках кровяных сосудов повышается степень проницаемости, что в итоге сказывается на работе всего организма.
Диагностику гипоплазии может проводить лишь профессионал при заборе целой серии анализов. Самостоятельно определить заболевание почти невозможно, да и симптомы развития схожи сразу с несколькими опасными нарушениями в работе организма. Если диагноз был поставлен, специалисты сразу рекомендуют переходить к лечению, поскольку гипоплазия — болезнь опасная, и чем раньше с ней начать бороться, тем будет лучше.
Лечение болезни
Гипоплазия костного мозга — это заболевание очень опасное, и оно требует немедленного врачебного вмешательства. Обычно лечение подразумевает иммуносупресивную терапию, направленную на восстановление количества стволовых клеток и улучшение их функционирования. При наличии тяжелых патологий печени или крайних степеней развития инфекционных заболеваний, иммуносупресивная терапия может быть заменена на другие методики лечения.

В таких случаях проводится трансплантация костного мозга. К данной методике врачи могут прибегнуть и в том случае, если костный мозг оказался сильно поражен болезнью. Брать костный мозг для трансплантации можно лишь после серии анализов, подтверждающих сходство биологических материалов. Если костный мозг не подойдет человеку, произойдет его постепенное отторжение.
Если иммуносупресивная терапия не дает результатов, врачи прибегают к спленэктомии, то есть операции по удалению селезенки. Так как селезенка является главным источником иммуногенеза, ее удаление зачастую позитивно сказывается на улучшении самочувствия.
Что такое гипоплазия костного мозга — вопрос, который задают многие люди после постановки диагноза. Лечение данной болезни протекает очень тяжело, и для полного избавления от симптомов необходимо проводить курс длиною в 9-12 месяцев. Далеко не всегда даже столь длительная терапия оказывается эффективной. Если все врачебные методики оказываются бесполезными, а болезнь продолжает прогрессировать, доставляя немалый дискомфорт, человеку остается лишь прибегнуть к хирургическому вмешательству.
Пересадка костного мозга в подавляющем большинстве случаев помогает эффективно избавиться от признаков заболевания. Лечение гипоплазии должно осуществляться исключительно специалистами, и перспектива самолечения народными методами приведет лишь к прогрессу гипоплазии.
Столь серьезные болезни, как гипоплазия костного мозга требуют срочного врачебного вмешательства. Поскольку признаки гипоплазии проявляются не сразу, человеку не стоит медлить при постановке диагноза, ведь в деле борьбы с такой патологией важна каждая затраченная на лечение минута.
http://provizor.org/node/47646
Панцитопения. Гипоплазия костного мозга
Панцитопения — это дефицит всех типов клеток крови, в том числе белых кровяных клеток, эритроцитов и тромбоцитов. Это состояние наступает, когда организм не может производить достаточное количество клеток крови, поскольку стволовые клетки костного мозга, формирующие клетки крови, не функционируют нормально.
Панцитопения имеет обширные последствия для всего организма, приводя к нехватке кислорода, а также вызывает проблемы с иммунной функцией. Апластическая анемия или панмиелофтиз — другие названия панцитопении.
Формы и симптомы панцитопении
Панцитопения обычно происходит в двух формах: идиопатическая, причина которой не известна, но часто носит аутоиммунный характер (означает, что тело атакует собственные ткани, как посторонние вещества) и вторичная, вызванная факторами окружающей среды.
Примерно половина всех случаев панцитопении относится к идиопатическим. Кроме того, вирусные инфекции, радиация и химиотерапия, а также реакция организма на лекарственные препараты и воздействие токсинов может ускорить развитие панцитопении.
Форма заболевания с пороками развития может определяться как врожденная, то есть передающаяся по наследству. Нарушения в работе костного мозга еще в утробе матери приводят к тому, что рождается ребенок с нарушением различных систем и внутренних органов.
Общие симптомы панцитопении: усталость, слабость, проявление кожных дефектов, например, высыпания или несвежий вид «помятой» кожи. Может присутствовать кровотечение из носа, десен, а также кровотечения внутренних органов.
Дополнительные симптомы: бледность, частые вирусные инфекции, бледная кожа, тахикардия, сбивчивое дыхание, кровоподтеки на поверхности кожи, слабость.
Причины панцитопении и факторы риска
Панцитопения может быть вызвана наследственными причинами (генными мутациями), лекарственными препаратами или воздействием таких факторов среды, как радиация или мышьяк. Примерно в половине случаев панцитопении заболевание имеет идиопатическую форму, и точную его причину установить не удается. В основе может лежать аутоиммунное нарушение, при котором организм разрушает собственные клетки и ткани как посторонние вещества или примеси в окружающей среде. В очень редких случаях к этому состоянию может привести беременность.
Определение причины очень важно для врача, поскольку от этого будет зависеть методика лечения. Например, панцитопения, вызванная экологическим фактором, может регулироваться при помощи удаления отравляющего вещества и нормализации условий проживания.
Факторы риска развития панцитопении
Ряд факторов увеличивает риск развития панцитопении, однако не все люди, проживающие в условиях повышенного риска или подвергающиеся воздействию факторов, заболевают.
Вещества и факторы, чаще всего вызывающие панцитопению:
- взаимодействие с токсинами окружающей среды, например, бензолом или мышьяком;
- семейная история заболеваний крови;
- волчанка или некоторые другие аутоиммунные заболевания;
- беременность (очень редко);
- лучевая терапия;
- антибиотики, иммунодепрессанты.
- химиотерапевтические препараты;
- радиация;
- вирусные инфекции.
Лечение панцитопении
Врожденная форма панцитопении лечится по схеме, которую определяет врач в каждом отдельном случае. При легких или умеренных проявлениях лечение может быть не обязательным, однако при более серьезных формах заболевания актуально переливание крови (оно помогает восстановить баланс кровяных телец).
Однако с течением времени переливание крови теряет свою эффективность. Более радикальной мерой лечения является пересадка костного мозга или терапия стволовыми клетками. Эти процедуры восстанавливают способность костного мозга вырабатывать клетки крови. Такие процедуры, как правило, эффективны для молодых пациентов, но пожилым так же может быть полезным употребление препаратов, стимулирующих активность костного мозга.
В случаях, связанных с экологическими факторами, панцитопения может быть побеждена лишь устранением внешнего фактора — какого-либо токсина или отравляющего вещества.
Если основной причиной заболевания является атака иммунной системы на костный мозг, назначаются иммунодепрессанты:
- антитимоцитарные антитела, которые подавляют естественный иммунный ответ организма
- кортикостероиды, такие как метилпреднизолон;
- циклофосфамид (Цитоксан);
- циклоспорин (Sandimmune, Neoral).
Стимулирующие костный мозг препараты:
- эпоэтин альфа (Epogen, прокрит);
- филграстим (Нейпоген);
- Pegfilgrastim (Neulasta);
- Sargramostim (Leukine, Prokine).
Каковы потенциальные осложнения, вызываемые панцитопенией?
При отсутствии лечения панцитопения может привести к опасным для жизни кровотечениям и развитию инфекций. Осложнения чаще бывают у пожилых больных.
Гипоплазия костного мозга: симптомы и лечение
Гипоплазия, или недостаточность костного мозга, — это группа расстройств, приобретенных или наследственных. Они подразумевают расстройства кроветворной системы, в том числе дефицит тромбоцитов, эритроцитов, миелоидных клеток.
Унаследованные формы недостаточности костного мозга это: анемия Фанкони, дискератоз врожденный, анемия Даймонда-Блекфена и другие генетические заболевания. Наиболее распространенной причиной приобретенной гипоплазии костного мозга является апластическая анемия. Заболевания, которые появляются в результате приобретенной гипоплазии костного мозга: миелодиспластический синдром, пароксизмальная ночная гемоглобинурия и гранулярный лимфолейкоз.
Пациенты с недостаточностью костного мозга имеют малое количество крови по сравнению со здоровыми пациентами. Снижение числа тромбоцитов делает пациентов предрасположенными к спонтанному кровотечению из порезов и травм кожи, а также повышает кровоточивость слизистых оболочек. Заболевание развивается медленно, в течение несколько месяцев.
Наследственная гипоплазия костного мозга обычно диагностируется у молодых пациентов, а также у пациентов старше 60 лет.
Любое из этих заболеваний может сигнализировать о гипоплазии костного мозга: гематологическая цитопения, необъяснимый макроцитоз, миелодиспластический синдром или острый миелолейкоз, плоскоклеточный рак.
Для лечения гипоплазии костного мозга используются препараты, которые обычно назначаются при анемии, однако они редко бывают эффективными. Обычно их используют как вспомогательные средства, а основное лечение проводят при помощи:
- кортикостероидов;
- переливания крови (необходимо проводить с интервалами, поскольку процедура вызывает привыкание и оказывается не такой полезной для организма).
Некоторые случаи этого заболевания эффективно лечатся при помощи спленэктомии.
По материалам:
2015 Healthgrades Operating Company, Inc.
National Center for Biotechnology Information, U.S. National Library of Medicine
1994-2015 by WebMD LLC.

Как после новогодних праздников восстановить нормальную работу организма?

Почему носовая слизь полезна для здоровья?

Какие микроорганизмы живут в магазинных тестерах косметики?

Что общего между чипсами и бытовыми чистящими средствами?

Почему нужно употреблять рыбий жир каждый день?

Искусственное мясо, идентичное натуральному

Бесполезные лекарства или лекарства, которые не стоят ваших денег

Лазерная динамическая эпиляция: революция в борьбе с нежелательными волосами

Лучший способ бросить курить

Гомеопатия — надо ли ее запрещать?
- Лимфоидный лейкоз — что это такое? Причины появления, виды, симптомы, лечение — ключевые факты о лимфоидном лейкозе. Строение кости, костный мозг и образование клеток крови, их виды и функции. Виды лимфолейкоза. Факторы риска заболевания, симптомы лимфолейкоза, методы лечения
- Что такое множественная миелома и экстрамедуллярная плазмоцитома? — описание, механизм возникновения. Диагностика злокачественных заболеваний плазматических клеток, тесты для выявления множественной миеломы, ее симптомы. Химиотерапия множественной миеломы
- Геморрагические состояния. Синдром Эванса — синдром Эванса как сочетание тромбоцитопении, аутоиммунной гемолитической анемии и нейтропении, причины аутоиммунного заболевания. Симптомы синдрома Эванса, методы лечения
- Полицитемия — увеличение числа эритроцитов, уровня гемоглобина и общего объема эритроцитов, классификация, распространенность и клинические проявления
- Что такое синдром Имерслунд-Гресбека (мегалобластная анемия)? — причины, механизм возникновения, симптомы синдрома. Врожденный дефицит внутреннего фактора как вид мегалобластной анемии. Симптомы нарушения усвоения витамина В12, лечение
http://www.medicinform.net/haemo/haemo26.htm
Парциальная («красноклеточная») гипоплазия костного мозга. Эритробластофтиз
Особый интерес представляют случаи гипо-апластической анемии, протекающей с избирательным поражением эритропоэза, при сохранном тромбоцитопоэзе и отчасти лейкопоэзе.
Подобная форма (неправильно обозначаемая некоторыми авторами как «парциальная гипопластическая анемия» (представляет собой особый вариант гипопластической анемии, характеризующейся в отличие от тотального миелофтиза парциальной, «чисто красноклеточной» гипоплазией костного мозга.
Костномозговой пунктат в этих случаях представляет своеобразную картину эритробластофтиза, т. е. полного отсутствия эритробластических элементов при сохранении мегакариоцитов и элементов лейкопоэза («чисто белоклеточный» костный мозг, табл. 25).
От эритробластофтиза как проявления парциальной гипоплазии костного мозга следует отличать состояние острой эритробластопении, возникающей при функциональном истощении костного мозга, в частности при арегенераторных кризах, осложняющих течение гемолитических анемий (см. ниже). Морфологической особенностью «пении» (не «фтиза») является сохранение базофильных резервов кроветворения — эритробластов, обеспечивающих наступление гематологической ремиссии.
Картина крови. При парциальной «красно-клеточной» гипоплазии костного мозга изменения крови характеризуются тяжелой нор-мохромной или умеренно гиперхромной, макроцитарной анемией при нормальном лейкоцитозе или умеренной лейкопении с лимфоцитозом и нормальном тромбоцитозе. Анемия носит гиперсидеремический характер, нередко осложняясь гемосидерозом органов.
Этиология. Этиология парциальной «красноклеточной» гипоплазии костного мозга должна рассматриваться в плане специфического фактора (или факторов), оказывающих избирательно угнетающее действие на процессы эритропоэза.
В части случаев эритробластофтиза нельзя отвергнуть влияние экзогенных факторов — хронических интоксикаций, инфекций, повторных кровопотерь или длительного гемолиза, приводящих в конечном итоге к истощению костномозгового «эритрона». Таков, по-видимому, генез парциальной, «красно-клеточной» гипоплазии костного мозга при «железном диабете» — хронической гемосидеринурии с пароксизмальной ночной гемоглобинурией (ПНГ — болезнь Мариафа-ва) и других состояниях, сопровождающихся развитием вторичного эритробластофтиза.
Особое внимание привлекает проблема «чистой красноклеточной» гипоплазии костного мозга в связи с описанием подобных случаев, нередко в сочетании с гипогаммаглобулинемией и миастенией, при доброкачественных опухолях вил очковой железы типа лимфоэпителиомы Шминке.
Доказанная в последние годы роль вилочковой железы в иммуногенезе, а также обнаружение у больных парциальной гипоплазией костного мозга антиэритроцитарных антител позволяют думать об иммунном, аутоагрессивном патогенезе данной анемической формы.
Лечение. Терапия парциальных гипоплазии костного мозга обычными противоанемиче-скими средствами (витамины комплекса В, препараты железа) не эффективна. Эритроцитотрансфузия оказывает лишь временный эффект. Следует помнить о том, что длительное применение препаратов железа и переливаний эритроцитной массы чревато возможностью развития гемохроматоза. Более эффективно применение кортикостероидной терапии.
В отдельных случаях ремиссия наступала после спленэктомии.
При анемии, развивающейся у больных с опухолью вилочковой железы, радикальным методом лечения является операция — тимэктомия. По данным Havard (1964), положительный результат от тимэктомии был получен у 14 из 23 больных.
http://studfiles.net/preview/1785623/page:30/
Аплазия костного мозга: что это такое и какими симптомами сопровождается
Аплазия костного мозга (аплазия кроветворения) – синдромы костномозговой недостаточности, которые характеризуются подавлением функций кроветворения. У пациентов наблюдается дефицит всех видов кровяных клеток: лейкоцитов, эритроцитов и тромбоцитов. Первопричина аплазии кроветворения выявляется с помощью лабораторных методов. Способы лечения зависят от болезни, которая вызвала патологию. В международной классификации болезней (МКБ-10) аплазия костного мозга обозначается кодом D61.
Что такое аплазия костного мозга?
Костный мозг – орган кроветворной системы, который содержит как стволовые, так и созревшие клетки крови. Уменьшение количества всех клеток крови из-за приобретенной (часто) или врожденной (редко) аплазии костного мозга называется апластической анемией. Врожденные формы включают анемию Фанкони и синдром Даймонда-Блекфена.
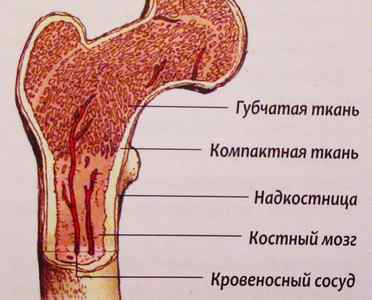
Аплазия костного мозга – состояние, при котором кроветворная функция костного мозга резко подавлена
Ежегодно возникает 0,2-0,3 случая на 100 000 человек. Около 200-300 человек в России страдают аплазией костного мозга. Болезнь опасна для жизни и отражается в измененной картине крови пациентов. Диагноз может затронуть даже здоровых молодых людей.
Если нарушается гемопоэз в костном мозге, могут образовываться дефектные кровяные клетки. Расстройство может затрагивать разные типы клеток (эритроциты, лейкоциты, тромбоциты). Симптомы аплазии кроветворной системы возникают потому, что количество клеток уменьшается настолько, что они не могут выполнять свою функцию в достаточной степени.
Классификация
По клиническому течению различают острую (до 1 месяца), подострую (от 1 до 6 месяцев) и хроническую форму (от полугода и дольше) заболевания. По тяжести грануло- и тромбоцитопении выделяют 3 степени:
Уменьшение концентрации эритроцитов вызывает слабость, усталость, одышку и учащенное сердцебиение, особенно во время физических нагрузок. У пациентов с анемией часто наблюдается бледность кожных покровов.

При аплазии костного мозга иммунная система снижается
Из-за уменьшения количества белых кровяных телец повышается восприимчивость к инфекционным заболеваниям. Поскольку иммунная система организма не может оптимально работать с уменьшенным количеством гранулоцитов, инфекция может привести к фатальным последствиям. Поэтому важно обратиться незамедлительно к врачу в таких ситуациях.
При уменьшенном количестве тромбоцитов нарушается свертывающая система крови. В результате возникают так называемые петехии – очень небольшое точечное кровотечение или кровоподтеки (гематома). Они также могут возникать спонтанно, без предварительной травмы. Даже относительно небольшое кровотечение или микротравма (например, при посещении стоматолога) может привести к летальному исходу.
По этиологии (причине возникновения) выделяют врожденную и приобретенную аплазию костного мозга.
- Анемия Фанкони.
- Синдром Даймонда-Блекфена.
- Идиопатическая (>70% случаев).
- Лекарственная (10%): нестероидные противовоспалительные средства, хлорамфеникол, фенилбутазон, золото, пеницилламин, аллопуринол, фенитоин.
- Токсическая (10%).
- Вирусная (5%): особенно парвовирус B19 и вирус Эпштейна-Барр.
Поскольку во многих ситуациях фактор риска не может быть определен, большинство случаев заболевания следует классифицировать как идиопатические – без известной причины. Однако гипоплазия (или аплазия) костного мозга также может возникать как часть аутоиммунного заболевания, такого как системная красная волчанка.
Известно, что ряд цитотоксических препаратов увеличивает риск развития гипоплазии в области костного мозга. Следует отметить, что антиметаболиты вызывают только острую аплазию, тогда как алкилирующие вещества – хроническую.
Опасные осложнения
Гипоплазия, как и аплазия, костного мозга может протекать остро или хронически. Первыми предупредительными признаками могут быть нейтропения и тромбоцитопения. Иногда возникают клинические признаки анемии: усталость, общее чувство слабости, бледность кожи и слизистых оболочек. При хронической форме развиваются инфекции в области рта и шеи. Иногда увеличивается склонность к кровотечениям.
Диагностика
При физикальном осмотре больного определяют частоту пульса, так как при аплазии чаще всего он учащен
Вначале врач собирает анамнез, а затем проводит физический осмотр пациента. При подозрении на аплазию костного мозга назначают следующие обследования:
- Анализ крови.
- Гистологическое исследование.
- Цитогенетическое исследование.
При микроскопическом анализе выявляются «пустоты» в костном мозге. Это означает, что гемопоэтические клетки, которые содержатся у здоровых людей, отсутствуют и частично заменены жировыми клетками у пациентов с аплазией кроветворной системы.
Однако значительное снижение таких клеток также наблюдается при других заболеваниях. Врожденная недостаточность костного мозга или миелодиспластический синдром – распространенные причины гипоплазии кроветворной системы. Поэтому необходимы дальнейшие исследования, чтобы подтвердить диагноз.
Чтобы исключить лейкоз или миелодиспластический синдром и другие причины, может потребоваться цитогенетическое исследование. Возможные отклонения в количестве, а также в структуре хромосом могут быть обнаружены с помощью этого метода исследования. Приобретенная форма болезни обычно не характеризуется дефектами генетического материала. Выявление изменений в хромосомах, скорее всего, указывает на наличие миелодиспластического синдрома.
Если известен фактор, вызывающий анемию – излучение, химические вещества, лекарства, – рекомендуется его устранить. Лечение зависит от тяжести заболевания. Терапия тяжелой и очень тяжелой аплазии кроветворной системы не отличается.
При легкой форме аплазии рекомендуется выжидательная терапия: пациент должен регулярно посещать врача и проходить плановые обследования. Ожидаемая продолжительность жизни этих пациентов не уменьшается даже при отсутствии лечения.
При тяжелой и очень тяжелой аплазии костного мозга назначают следующие терапевтические меры:
- Трансплантация гемопоэтических стволовых клеток.
- Иммунодепрессивная терапия.
- Поддерживающая терапия.
Если имеется донор в семье (например, братья и сестры), пересадку костного мозга следует выполнить как можно скорее. Длительное ожидание перед трансплантацией и большое количество переливаний крови могут ухудшить исходное состояние пациента. Если не найдено подходящего донора, назначается иммунодепрессивная терапия. Предварительное планирование лечения в специализированном центре абсолютно необходимо при аплазии костного мозга.
При аллогенной трансплантации пациент получает стволовые клетки крови от другого человека. Предшественники клеток крови могут принадлежать родственнику или незнакомцу. Аллогенная пересадка незнакомого донора связана с относительно более высокими рисками из-за низкой совместимости тканей.
Иммуносупрессивная терапия

Иммуносупрессивное лечение проводится, если нельзя провести трансплантацию
Если подходящий донор не найден, рекомендуется проведение иммуносупрессивной терапии. В этом случае комбинация нескольких препаратов подавляет дефектную иммунную реакцию, которая привела к уменьшению кроветворных клеток в костном мозге.
В последние годы назначают комбинацию антитимоцитарного глобулина и циклоспорина. В течение первых 4 дней стационарного лечения антитимоцитарный глобулин вводят через вену. Кроме того, пациенты получают в течение 4 недель глюкокортикоидное средство. Как только у пациента улучшается самочувствие и показатели крови, его можно отпустить домой и давать лекарства в виде таблетки или жидкости.
После иммунодепрессивной терапии у около 30% пациентов возникает рецидив болезни. У около 20% пациентов развивается острый миелоидный лейкоз или пароксизмальная ночная гемоглобинурия. Если в первые 3-6 месяцев после введения препаратов не наблюдается заметного улучшения состава крови или после успешной терапии апластическая анемия снова рецидивирует, необходима трансплантация стволовых клеток. Повторная иммуносупрессивная терапия, как правило, не проводится.
Поддерживающая терапия
В зависимости от типа лечения (трансплантация костного мозга или применение иммунодепрессивных препаратов) требуется использовать различные поддерживающие меры, которые помогают бороться с побочными эффектами или осложнениями болезни. Иногда назначают симптоматические средства для уменьшения усталости.
Шансы на выздоровление пациента при своевременно начатом лечении достаточно высокие, хотя это опасное для жизни состояние. Аллогенная трансплантация гемопоэтических стволовых клеток приводит к выздоровлению 80-90% пациентов с гипоплазией в области костного мозга. Пересадка клеток от незнакомого донора также может вылечить пациентов с заболеваниями костного мозга. Однако у многих детей и подростков (около 20-30%) по-прежнему развиваются серьезные, а иногда и фатальные осложнения.
После завершения трансплантации пациенты должны обследоваться не реже одного раза в год у специалиста. Плановые обследования помогают своевременно лечить и предотвращать долгосрочные осложнения.