Гипоплазия костного мозга — что за болезнь
Вопрос №6 — Что такое гипоплазия костного мозга?
Артемьева Вероника из Нижнего Тагила спрашивает:
Что такое гипоплазия костного мозга, и какими симптомами сопровождается это заболевание?
Ответ эксперта:
Гипоплазия костного мозга – это состояние, при котором миелоидная ткань замещается жировой. Само понятие «гипоплазия» в переводе означает недостаточность формирования. При недостаточном формировании миелоидной ткани нарушается функция красного костного мозга, в результате чего значительно снижается выработка кровяных клеток – лейкоцитов, эритроцитов, тромбоцитов. Недостаточность костного мозга является одной из разновидностей панцитопении.
Причины развития
Существует две формы болезни:
Причиной развития наследственных форм являются следующие патологии:
- анемия Фанкони;
- врожденный дискератоз;
- анемия Даймонда-Блекфена;
- другие генетические заболевания.
Недостаточность выработки кровяных клеток может выступать в качестве самостоятельного заболевания при апластической анемии или развиваться на фоне следующих заболеваний:
- цирроза печени;
- хронического гепатита;
- злокачественных новообразований;
- различных аутоиммунных расстройств.

Проявления болезни
В организме больных людей объем крови гораздо ниже, чем у здоровых. В результате снижения количества тромбоцитов, у пациентов возникают спонтанные кровотечения. Опасность могут представлять любые порезы, травмы, приводящие к значительной потере крови. Кровоточивости подвержены слизистые оболочки и внутренние органы.
Недостаточность выработки лейкоцитов приводит к снижению иммунитета, способствующего возникновению частых инфекционных заболеваний.
Принципы лечения
Лечением данной патологии занимается врач-гематолог. Выбор способа терапии зависит от причины возникновения болезни. Апластическую анемию возможно устранить только путем пересадки костного мозга. Если не удается найти подходящего донора, больному показан прием препаратов, угнетающих иммунную систему (Циклоспорина А). Иммунодепрессивная терапия позволяет добиться успеха только при нетяжелых формах болезни.
Всем без исключения пациентам производят внутривенное введение тромбоцитарной и эритроцитарной массы. В целях предотвращения развития инфекционных и грибковых поражений больным назначается прием антибактериальных и противогрибковых препаратов.
Одной из причин недостаточного содержания кровяных клеток является повышение активности селезенки – гиперспленизм. Поэтому пациентам может быть проведена спленэктомия – операция, в ходе которой производят удаление селезенки.
Видео: Что такое трансплантация костного мозга
http://serdechka.ru/voprosy-otvety/gipoplaziya-kostnogo-mozga.html
Парциальная («красноклеточная») гипоплазия костного мозга. Эритробластофтиз
Особый интерес представляют случаи гипо-апластической анемии, протекающей с избирательным поражением эритропоэза, при сохранном тромбоцитопоэзе и отчасти лейкопоэзе.
Подобная форма (неправильно обозначаемая некоторыми авторами как «парциальная гипопластическая анемия» (представляет собой особый вариант гипопластической анемии, характеризующейся в отличие от тотального миелофтиза парциальной, «чисто красноклеточной» гипоплазией костного мозга.
Костномозговой пунктат в этих случаях представляет своеобразную картину эритробластофтиза, т. е. полного отсутствия эритробластических элементов при сохранении мегакариоцитов и элементов лейкопоэза («чисто белоклеточный» костный мозг, табл. 25).
От эритробластофтиза как проявления парциальной гипоплазии костного мозга следует отличать состояние острой эритробластопении, возникающей при функциональном истощении костного мозга, в частности при арегенераторных кризах, осложняющих течение гемолитических анемий (см. ниже). Морфологической особенностью «пении» (не «фтиза») является сохранение базофильных резервов кроветворения — эритробластов, обеспечивающих наступление гематологической ремиссии.
Картина крови. При парциальной «красно-клеточной» гипоплазии костного мозга изменения крови характеризуются тяжелой нор-мохромной или умеренно гиперхромной, макроцитарной анемией при нормальном лейкоцитозе или умеренной лейкопении с лимфоцитозом и нормальном тромбоцитозе. Анемия носит гиперсидеремический характер, нередко осложняясь гемосидерозом органов.
Этиология. Этиология парциальной «красноклеточной» гипоплазии костного мозга должна рассматриваться в плане специфического фактора (или факторов), оказывающих избирательно угнетающее действие на процессы эритропоэза.
В части случаев эритробластофтиза нельзя отвергнуть влияние экзогенных факторов — хронических интоксикаций, инфекций, повторных кровопотерь или длительного гемолиза, приводящих в конечном итоге к истощению костномозгового «эритрона». Таков, по-видимому, генез парциальной, «красно-клеточной» гипоплазии костного мозга при «железном диабете» — хронической гемосидеринурии с пароксизмальной ночной гемоглобинурией (ПНГ — болезнь Мариафа-ва) и других состояниях, сопровождающихся развитием вторичного эритробластофтиза.
Особое внимание привлекает проблема «чистой красноклеточной» гипоплазии костного мозга в связи с описанием подобных случаев, нередко в сочетании с гипогаммаглобулинемией и миастенией, при доброкачественных опухолях вил очковой железы типа лимфоэпителиомы Шминке.
Доказанная в последние годы роль вилочковой железы в иммуногенезе, а также обнаружение у больных парциальной гипоплазией костного мозга антиэритроцитарных антител позволяют думать об иммунном, аутоагрессивном патогенезе данной анемической формы.
Лечение. Терапия парциальных гипоплазии костного мозга обычными противоанемиче-скими средствами (витамины комплекса В, препараты железа) не эффективна. Эритроцитотрансфузия оказывает лишь временный эффект. Следует помнить о том, что длительное применение препаратов железа и переливаний эритроцитной массы чревато возможностью развития гемохроматоза. Более эффективно применение кортикостероидной терапии.
В отдельных случаях ремиссия наступала после спленэктомии.
При анемии, развивающейся у больных с опухолью вилочковой железы, радикальным методом лечения является операция — тимэктомия. По данным Havard (1964), положительный результат от тимэктомии был получен у 14 из 23 больных.
http://studfiles.net/preview/1785623/page:30/
Гипоплазия кроветворения
Гипоплазия кроветворения может развиться как синдром при туберкулезном процессе, но наряду с этим туберкулез может сочетаться и с истинной ГА [Любимова Л. С., Турбина Н. С. и др., 1968; Ulku В. et al., 1982].
В качестве такого примера можно привести одно наше наблюдение.
Больной Г. К., 52 лет, считает себя больным с ноября 1967 г., когда впервые появились быстрая утомляемость, кашель и периодическое повышение температуры до 40 °С. В январе 1968 г. были выявлены снижение содержания гемоглобина до 40 г/л, лейко- и тромбопения. Диагностирована гипопластическая анемия. Проведено лечение гемотрансфузиями с положительным эффектом. В апреле 1969 г. ухудшение: снижение уровня гемоглобина, снова появился кашель.
Анализ крови: Нb 68 г/л, эр. 2,8*10 12 /л, л. 2,8*10 9 /л, лимф. 96%. Миелограмма: бл. 4%, лимф. 68,6%. Геморрагий не было, несмотря на стойкую тромбоцитопению. Лечение гемотрансфузиями (всего 13), преднизолоном по 30 мг/сут (всего 2 г) на этот раз оказалось малоэффективным. При поступлении в ЦНИИГПК 01.08.69 г. состояние средней тяжести. Кожные покровы бледны. Подкожный жировой слой развит слабо, склеры слегка иктеричны. Периферические лимфатические узлы, печень и селезенка не увеличены. Билирубин 8,5 мкмоль/л свободный, прямая проба Кумбса положительная. Миелограмма от 12.08.69 г.: бл. 3,4%, лимф. 83,2%, красный росток 3,8%, пл. кл. 0,4%, встречаются скопления ретикулярных клеток, остеокласты, мегакариоциты (единичные в препарате), в редких полях зрения — свободно лежащие единичные тромбоциты.
В трепанате костного мозга на фоне общего рассасывания костной ткани видны участки оживления эндоста. Некоторые полости заполнены тканью типа грануляционной, среди которой видны отдельные фибробласты, гистиоциты, лимфоидные элементы. В других полостях строма крупноячеистого строения с отдельными элементами фиброретикулярной ткани. Элементы нормального гемопоэза почти отсутствуют.
Среди единичных сегментоядерных лейкоцитов, элементов красного ряда видны крупные темные клетки и клетки с небольшим круглым ядром, богатым хроматином, дифференцировать которые не представляется возможным. Заключение: подобная картина может наблюдаться при неоплазме, туберкулезе, бруцеллезе и других хронических инфекциях.
Таким образом, полученные данные указывали на угнетение кроветворения при каком-то другом заболевании. Поскольку у больного было периодическое повышение температуры (до 38 — 39 °С) и кашель, в первую очередь требовалось исключить туберкулез легких.
Однако кроме петрифицированных лимфатических узлов слева, свежих изменений в легких не выявлено. При рентгенологическом исследовании желудочно-кишечного тракта патологии не обнаружено. Многократные посевы крови были отрицательными.
Сканографическое исследование печени также не облегчило диагностику. Состояние больного постепенно ухудшалось, он стал худеть, лихорадка оставалась на высоких цифрах, признаки депрессии гемопоэза нарастали, развились правосторонняя нижнедолевая пневмония, некротический стоматит. При явлениях сердечной слабости больной умер.
На аутопсии: цирротический туберкулез легких с милиарным распространением процесса (легкие, селезенка, лимфатические узлы, печень), вторичный миелофиброз с угнетением кроветворения, нижнедолевая правосторонняя пневмония.
Данное наблюдение демонстрирует несколько важных клинических аспектов и в первую очередь трудности в установлении основного заболевания. Тем не менее высокая лихорадка при обнаружении петрифицированных очагов в лимфатических узлах корня левого легкого и гистологическая картина костного мозга должны были навести на мысль о целесообразности использования антитуберкулезных средств, хотя бы потому, что у больного применялся преднизолон.
Эта история болезни может служить примером и того, насколько глубоким бывает угнетение гемопоэза при другом заболевании.
«Депрессии кроветворения», О.К.Гаврилов,
Ф.Э.Файнштейн, Н.С.Турбина
http://www.serdechno.ru/depres/gipoplasticheskie/differenc/9696.html
Sosudinfo.com
Патологическое состояние, характеризующееся сниженным содержанием клеток крови и гемоглобина, называется анемией (народный вариант – малокровие). Уменьшенный показатель гемоглобина является основным необходимым признаком для постановки диагноза. Снижение эритроцитов при анемии может не наблюдаться и к определяющему критерию не относиться. Важно знать, что анемия не самостоятельное заболевание, а лишь проявление (симптом) основной патологии. При снижении уровня гемоглобина в крови должна проводиться тщательная диагностика, чтобы обнаружить причину симптома. Анемия развивается на фоне повышенной кровопотери, сниженного образования гемоглобина, усиленного разрушения клеток крови. По данным критериям ее подразделяют на следующие виды:
Общие понятия о гипопластической анемии
Гипопластической анемией является патологическое изменение картины крови вследствие подавления работы красного костного мозга. Проявляется это снижением выработки всех ростков крови (эритроцитарного, лейкоцитарного, тромбоцитарного) или только красного (уменьшение эритроцитов). История первого описания и появления данного заболевания начинается с 1888 года. В это время П. Эрлих выявил у девушки болезнь, проявляющуюся острым развитием кровоточивости, лихорадки, глубокой анемии и лейкопении. По результатам вскрытия и исследования костного мозга, признаков нарушения кроветворения выявлено не было. Анапластическая анемия как самостоятельное заболевание выделено Шоффаром в 1904 г. Позднее появилась апластичная анемия по типу Эрлиха с симптомами сепсиса, некроза, геморрагии и аплазии (отсутствие всех ростков кроветворения в костном мозге), проявляющаяся у молодых людей (18–20 лет). Основным контингентом, страдающим от данного заболевания, являются юные девушки и дети. В патогенезе развития выделяют несколько этапов. Сначала ткани, вследствие нехватки кислорода и питательных веществ, атрофируются и утрачивают свои функции. Далее жировая и соединительная ткани замещают погибшие клетки, что приводит к распространению патологического процесса. Прогрессирование заболевания происходит очень быстро и в случае отсутствия терапии может привести к смерти.

Классификация
В зависимости от происхождения гипопластическая анемия бывает:
- врожденной. Симптомы заболевания проявляются в раннем детстве и быстро прогрессируют. Причинами развития могут явиться генетические мутации ДНК у плода; наследственная предрасположенность (есть данные о подобной аномалии у кого-либо из родственников); нарушенное внутриутробное развитие (патологические изменения в системе кроветворения плода под воздействием неблагоприятного фактора). Исследования показали, что мальчики страдают врожденным апластическим синдромом в два раза чаще девочек;
- приобретенной. Данный вид гипопластической анемии характерен для любой возрастной группе.
Существуют идиопатическая (причина заболевания неизвестна) и миелотоксическая (предпосылкой является токсическое действие внешнего фактора) формы. К причинам, определяющим развитие миелотоксической формы анемии, относят:
- хроническую интоксикацию химическими веществами;
- лекарственные препараты с побочным действием на кроветворение (гормональные, транквилизаторы, цитостатики);
- облучение организма высокими дозами радиации (подвержены рентгенологи);
- заболевания эндокринной системы (могут осложниться гипопластической анемией);
- воздействие вирусов на клетки крови;
- на фоне туберкулеза и беременности также может развиваться гипопластическая анемия, но такие случаи встречаются в медицинской практике редко.
В зависимости от длительности течения заболевания выделяют:

В зависимости от массивности поражения костномозговых функций существуют патологии:
В зависимости от пораженных ростков крови выделяются:
По международной классификации болезней (мкб-10), анапластическая анемия имеет код D60 (эритробластопения – приобретенная красноклеточная аплазия), D61 (другие апластические анемии).
Выделяют три группы главных причин развития гипопластической анемии:

Механизм повреждения костного мозга заключается в том, что под действием вышеперечисленных причин происходит изменение хромосомного набора, вызывающее нарушенный синтез ДНК. Образование клеток крови тормозится и ткань красного костного мозга замещается жировой, которая не способна выполнять продуцирующую функцию. Общее состояние больного ухудшается, а картина крови представляется панцитопенией.
Основные симптомы патологии
Патогенез проявлений данной болезни объясняется неспособностью клеток крови (из-за низкого их содержания) выполнять свои функции. Таким образом, появление геморрагического синдрома обусловлено тромбоцитопенией и повреждением сосудистой стенки (недостаток серотонина и гипоксия приводит к повышению ее проницаемости).
К основным проявлениям геморрагического синдрома относят:
- частые беспричинные носовые кровотечения;
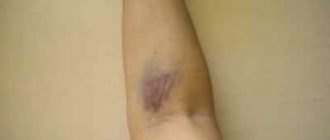
- появление кровоподтеков и синяков на коже при надавливании (пальцевая и манжеточная проба);
- кровотечение из десен;
- женщины часто жалуются на обильность и удлинение менструаций.
В случае затянувшегося патологического процесса или при массивном повреждении тромбоцитов могут развиваться такие осложнения, как профузное внутреннее кровотечение или инфаркт головного мозга с кровоизлиянием. В итоге это может привести к смерти больного.
Снижение иммунитета и сопротивляемости к инфекционным агентам связано с угнетением лейкоцитарного ростка. Гипопластическая анемия с иммунодефицитом представлена следующими симптомами:
Ребенок более подвержен таким изменениям, поскольку его организм находится на стадии активного роста и развития всех систем. Заболевание склонно к хронизации процесса с периодическими обострениями.

Уменьшенное образование эритроцитов приводит к развитию анемического симптомокомплекса:
В случае выявления остро протекающей тяжелой формы заболевания прогноз у такого пациента неблагоприятный: смерть наступает в течение 3 месяцев. Частой причиной летальности являются внутренние кровотечения или персистирующие инфекции, приводящие к сепсису.
Анализы крови и их расшифровка
Чтобы правильно поставить клинический диагноз, необходимо собрать анамнез, осмотреть пациента, провести пункцию костного мозга, исследовать кровь на признаки гипоплазии. Если при этом селезенка, лимфатические узлы и печень не увеличены, то можно выставить гипопластическую анемию.
Если это приобретенная форма заболевания, то анализ крови представлен:
- нормохромной (нет изменений цветового показателя), нормоцитарной (размеры эритроцитов в норме) анемией;
- содержание ретикулоцитов может быть сниженным или нормальным;
- лимфоцитопенией (уменьшена концентрация лимфоцитов), снижение происходит в большей степени за счет нейтрофилов;
- концентрация тромбоцитов снижена, что проявляется замедленным тромбообразованием и удлиненным временем кровотечения. При этом факторы свертывания в норме;
- происходит повышение общей железосвязывающей способности и сывороточного железа.

Если этиология заболевания имеет врожденный характер, то в крови выявляются следующие изменения:
- макроцитоз (увеличенный диаметр) эритроцитов;
- ретикулоцитопения (низкое содержание ретикулоцитарных клеток);
- показатель тромбоцитов и лейкоцитов в норме.
Апластическая анемия не поддается полному излечению. При выявлении на начальных этапах развития, правильной дифференциальной диагностике и своевременно начатом лечении можно добиться остановки прогрессирования патологии.
Лечение гипопластической анемии
Лечение заболевания проводят в зависимости от тяжести, степени выраженности проявлений и формы патологии. Выделяют следующие методы:
Консервативные
Оперативные
- при врожденной или аутоиммунной форме апластичного синдрома выполняют спленэктомию, что дает хороший результат;
- у лиц молодого возраста и в случае течения анапластического синдрома менее 3 месяцев производят пересадку костного мозга. Предварительно необходима диагностика донорского материала на НLA совместимость. До операции выполняется лучевая и иммуносупрессивная терапия.
Гипопластическая анемия является неизлечимой патологией, но при правильном лечении и выполнении рекомендаций доктора можно остановить прогрессирование заболевания и предупредить развитие осложнений. Выявив нарушенное кроветворение на начальных этапах, и проводя его правильное лечение, можно улучшить прогноз исхода событий.
http://sosudinfo.com/malokrovie/osobennosti-gipoplasticheskoj-anemii.html
Заболевания системы кроветворения. Гипопластическая и апластическая анемия
В основе заболевания лежит угнетение кроветворения, нарушение пролиферации элементов гемопоэза. Выделяют острую и подострую апластическую и гипопластическую анемию, хроническую гипопластическую анемию, гилопластическую анемию с гемолитическим компонентом.
Этиология. Определенную роль в возникновении заболевания играют эндогенные (эндокринные), экзогенные (химические, физические, токсико-аллергические, инфекционные) факторы.
Патогенез. В патогенезе важную (главную) роль играет нарушение процессов метаболизма в кроветворных клетках (понижение усвоения железа эритробластами костного мозга), синтеза гемоглобина.
Клиника и диагностика. Клиническая симптоматика острой апластической и гипопластической анемии, помимо выраженного малокровия, характеризуется кровоточивостью по типу тромбошпопенической пурпуры, анемией, лейкопенией, тромбоцитопенией.
Для апластической анемии характерно бурное нарастание анемизации со значительным снижением гемоглобина (30-60 г/л), эритроцитов (1-2х10,2/л), лейкоцитов (0,4-1,0х 109/л) (с лимфоцитозом 60-80%), тромбоцитов — до нуля. В разгаре заболевания нередко наблюдаются кровоизлияния в мозг, склеру и дно глаза.
При подострой гипопластической анемии геморрагические проявления выражены нерезко или отсутствуют. Гемограмма, миелограмма изменены несколько меньше. Течение хронической гипопластической анемии длительное с частыми обострениями. Эта форма анемии иногда сопровождается гемолитическим компонентом. При гипо- и апластических анемиях печень и селезенка, как правило, не увеличены. В костном мозге выявляются очаги гипоплазии кроветворения, выполненные жиром костномозговые полости и единичные участки кроветворения. Дифференциальный диагноз проводят с эритромиелозом.
Лечение. Показаны периодические переливания крови и ее компонентов: эритроцитной, лейкоцитной и тромбоцитной массы.
С гемостатической целью производят переливание плазмы, вводят эпсилонаминокапроновую кислоту, фибриноген, дицинон, проводят витаминотерапию (витамины группы В, никотиновая, фолиевая кислоты). В целях стимуляции гемопоэза назначают кортикостероидные гормоны (преднизолон и его аналоги в дозе 1-2 мг/кг), анаболические стероиды (нерабол, ретаболил и др.). Применяют трансплантацию костного мозга с тщательным серологическим подбором донора.
При прогрессировании анемии, геморрагическом синдроме, отсутствии эффекта от консервативного лечения, присоединении иммунного компонента и наличии антител к клеткам крови, а также при невозможности трансфузионной терапии показана спленэктомия. Во время и после оперативного вмешательства проводят переливание крови и ее компонентов, плазмы и др.
Послеоперационная летальность высока. Наиболее высокая летальность (37%) отмечается в первый год после операции, особенно у оперированных в фазе выраженного геморрагического криза (Л.С. Цепа, 1988).
Перейти к списку условных сокращений
Заболевания костного мозга: как лечить гипоплазию костного мозга?
При гипоплазии костного мозга, больной борется с сильнейшей анемией и угнетением костномозгового кроветворения. Как проявляется данное заболевание, и можно ли его вылечить?

Гипоплазия костного мозга — заболевание довольно редкое, и проявляется оно преимущественно у тех молодых людей, что не достигли по возрасту сорока лет. Какие симптомы при гипоплазии костного мозга встречаются, и может ли заболевание довести до летального исхода?
Как проявляется гипоплазия
Гипоплазия костного мозга — весьма опасное заболевание, и проявляется оно постепенно. Больные начинают жаловаться на одышку, постоянную усталость, шум в ушах и в боли в голове. Если на первые симптомы не обращать внимания, постепенно появятся небольшие подкожные кровоизлияния, а при развитии болезни человек начнет страдать из-за повышенной температуры и постоянной слабости.
Степень проявления тех или иных симптомов напрямую зависит от степени угнетения костномозгового кровопотока. Само заболевание сначала никак не проявляет себя, а болезненные признаки возникают уже на поздних этапах гипоплазии.

Геморрагические осложнения также наблюдаются на поздних этапах развития заболевания. К тому же, в стенках кровяных сосудов повышается степень проницаемости, что в итоге сказывается на работе всего организма.
Диагностику гипоплазии может проводить лишь профессионал при заборе целой серии анализов. Самостоятельно определить заболевание почти невозможно, да и симптомы развития схожи сразу с несколькими опасными нарушениями в работе организма. Если диагноз был поставлен, специалисты сразу рекомендуют переходить к лечению, поскольку гипоплазия — болезнь опасная, и чем раньше с ней начать бороться, тем будет лучше.
Лечение болезни
Гипоплазия костного мозга — это заболевание очень опасное, и оно требует немедленного врачебного вмешательства. Обычно лечение подразумевает иммуносупресивную терапию, направленную на восстановление количества стволовых клеток и улучшение их функционирования. При наличии тяжелых патологий печени или крайних степеней развития инфекционных заболеваний, иммуносупресивная терапия может быть заменена на другие методики лечения.

В таких случаях проводится трансплантация костного мозга. К данной методике врачи могут прибегнуть и в том случае, если костный мозг оказался сильно поражен болезнью. Брать костный мозг для трансплантации можно лишь после серии анализов, подтверждающих сходство биологических материалов. Если костный мозг не подойдет человеку, произойдет его постепенное отторжение.
Если иммуносупресивная терапия не дает результатов, врачи прибегают к спленэктомии, то есть операции по удалению селезенки. Так как селезенка является главным источником иммуногенеза, ее удаление зачастую позитивно сказывается на улучшении самочувствия.
Что такое гипоплазия костного мозга — вопрос, который задают многие люди после постановки диагноза. Лечение данной болезни протекает очень тяжело, и для полного избавления от симптомов необходимо проводить курс длиною в 9-12 месяцев. Далеко не всегда даже столь длительная терапия оказывается эффективной. Если все врачебные методики оказываются бесполезными, а болезнь продолжает прогрессировать, доставляя немалый дискомфорт, человеку остается лишь прибегнуть к хирургическому вмешательству.
Пересадка костного мозга в подавляющем большинстве случаев помогает эффективно избавиться от признаков заболевания. Лечение гипоплазии должно осуществляться исключительно специалистами, и перспектива самолечения народными методами приведет лишь к прогрессу гипоплазии.
Столь серьезные болезни, как гипоплазия костного мозга требуют срочного врачебного вмешательства. Поскольку признаки гипоплазии проявляются не сразу, человеку не стоит медлить при постановке диагноза, ведь в деле борьбы с такой патологией важна каждая затраченная на лечение минута.
http://provizor.org/node/47646
Идиопатическая гипоплазия гемопоэза
Для начала вот несколько определений:
Гемопоэз — это процесс образования, развития и созревания клеток крови.
Гипоплазия — недоразвитие органа, ткани.
Гипоплазия гемопоэза – это нарушение образования (снижение) клеток крови в костном мозге.
Идиопатической гипоплазия называется в том случае, если не установлена причина такого патологического процесса. Гипоплазия кроветворения может сопровождаться неэффективным гемопоэзом. В этом случае нарушается созревание и выход в кровяное русло клеток крови и происходит их гибель в костном мозге. Идиопатическая гипоплазия гемопоэза может затрагивать одновременно все ростки красной и белой крови (мегакариоцитарный, эритроцитарный и гранулоцитарный) и вследствие этого проявляться таким состоянием, как панцитопения – снижением содержания в крови всех ее клеточных элементов (эритроцитов, тромбоцитов, нейтрофилов). А может затрагивать какой-нибудь один росток, например, гранулоцитарный (агранулоцитоз). Идиопатическая гипоплазия гемопоэза обычно приводит к развитию такого заболевания, как гипопластическая (апластическая) анемия.
Гипопластическая (апластическая) анемия проявляется определенным комплексом симптомов:
1. Признаки анемии (снижения содержания эритроцитов в крови): кожные покровы бледные, больного беспокоит общая слабость и сердцебиение, одышка, при аускультации определяется систолический шум на верхушке.
2. Признаки тромбоцитопении, то есть снижения содержания тромбоцитов в крови ниже физиологической нормы (различные кровотечения, синяки на коже после ушиба и щипка – положительный симптом щипка, мелкототечные кровоизлияния).
3. Признаки нейтропении, то есть снижения содержания нейтрофилов крови ниже физиологической нормы (подверженность различным инфекционным заболеваниям, развитие инфекционно-воспалительных заболеваний и некрозов, язвенных поражений в различных органах и системах).
Диагностика
Состояние костного мозга оценивается по его клеточному составу и процентному соотношению жировой и кроветворной ткани. Анализ записывается в виде таблицы – миелограммы. Для взятия биопсии костного мозга чаще всего выполняется стернальная пункция (пункция грудины). В пользу гипоплазии костного мозга свидетельствует снижение количества клеток всех кроветворных ростков (миелокариоцитов менее 40 на 10*9/л, бластных клеток менее 1%).
В клиническом анализе крови отмечается анемия (нормо-, гипохромная, арегенераторная или макроцитарная), снижение содержания тромбоцитов и лейкоцитов, увеличение скорости оседания эритроцитов.
Лечение гипопластической анемии неясного генеза обычно проводится с применением гормонотерапии глюкокортикоидами, цитостатиков, анаболических стероидов, эритропоэтипов. В некоторых случаях по показаниям проводится удаление селезенки, пересадка костного мозга. А также симптоматическая терапия.
Апластические и гипопластические анемии
Апластические и гипопластические анемии
Апластические и гипопластические анемии (панмиелофтиз, панмиелопарез) развиваются в результате глубокого угнетения кроветворения.
Этиология апластической и гипопластической анемии. В развитии апластической и гипопластической анемии играют роль своеобразная повышенная реактивность кроветворения на воздействие внешних факторов и врожденная недостаточность эндокринной системы.
Известны многие физические, химические и биологические вещества, угнетающие процесс кроветворения вплоть до полного опустошения костного мозга. К ним относятся: лекарственные вещества (амидопирин, метилтиоурацил, новэмбихин, тиофосфамид, сарколизин, 6-меркаптопурин и другие цитостатические препараты, а также стрептомицин, левомицетин и другие антибиотики), химические препараты (бензол, бензин, мышьяк, ртуть, висмут и др.), лучистая энергия (рентгеновы лучи, радий, изотопы), инфекции (сепсис, грипп, некоторые формы туберкулеза) и др.
Симптомы, течение апластической и гипопластической анемии. По течению заболевания различают острую и подострую апластическую, подострую гипопластическую и хроническую гипопластическую анемию.
Клиническая симптоматология, картина крови и костного мозга при обеих формах апластической анемии сходны.
Подострую и хроническую формы гипопластической анемии можно отличить по первоначальным признакам заболевания. В первом случае анемия развивается более или менее остро, в другом — незаметно, исподволь. Можно различать их по интенсивности нарастания симптомов и по реакции организма на терапевтические мероприятия. Но нередко эти различия выявляются не сразу и уловить их можно при непрерывном наблюдении за больным.
При гипоплазии кроветворения картина пунктата костного мозга, как правило, не показывает полного опустошения, и при подсчете миелокариоцитов число их нередко бывает близким к 60 000-100 000 в 1 мм3 крови, как у здорового человека. Однако качественная характеристика костномозгового пунктата свидетельствует о нарушении процессов созревания костномозговых элементов. Преобладают незрелые клеточные формы всех трех ростков кроветворения. Число мегакариоцитов резко уменьшено, отшнуровка тромбоцитов отсутствует, снижено и число зрелых гранулоцитов. Клетки красного ряда в большинстве своем представляют незрелые стадии — базофильные и полихроматофильные эритробласты, создающие своеобразный вид «синего» костного мозга. Число лимфоцитов в миелограмме повышено.
Изменения, развивающиеся в костном мозге при гипо — и апластических состояниях, не всегда находят отражение в результатах цитологического анализа стернального пунктата. Гистологическое исследование костного мозга, содержащегося в аспирированном материале (исследование «крошки»), позволяет уточнить степень угнетения гемопоэза и полнее охарактеризовать состояние костного мозга. При трепанобиопсии выявляется опустошение костного мозга за счет замещения деятельной паренхимы жировыми клетками.
Гипопластическая анемия и апластическая анемия являются фазами одного и того же заболевания. Наряду с изменением костномозгового кроветворения при этих заболеваниях закономерно выявляется уменьшение массы лимфатической ткани. В селезенке в большинстве случаев обнаруживаются атрофические изменения. Деструктивные процессы в печени, в ряде наблюдений заканчивающиеся развитием цирротических изменений, по-видимому, возникают вследствие гипоксии тканей в результате длительной анемизации больных.
В редких случаях гипопластическая анемия протекает с ретикулярной реакцией. Очаговость пролиферации недифференцированных клеток на фоне выраженной гипоплазии костного мозга при отсутствии каких-либо признаков лейкоза говорит против системного гиперпластического процесса.
Ахрестическая анемия
«Ахрестическая» анемия («ахрезия» — неиспользование) развивается при нарушении возможности использования организмом антианемического фактора. В настоящее время «ахрестическая» анемия рассматривается как вариант гипопластической анемии, протекающей с эритробластозом. Проэритробласты теряют способность усваивать витамин B12, вследствие чего приобретают мегалобластоидный характер. При этой форме анемии симптомы нарушения со стороны центральной нервной системы и характерные для болезни Аддисона — Бирмера нарушения желудочно-кишечного тракта отсутствуют. Развитие болезни постепенное. Анемия бывает гиперхромного типа с макроэритробластным кроветворением. Анемия резистентна к печеночной терапии.
Распознавание ахрестической анемии. апластической (гипопластической) анемии основывается на панцитопении, преобладании лимфоцитов в лейкоцитарной формуле, уменьшении общего количества ядерных элементов в пунктате костного мозга с нарушением их созревания.
В дифференциальной диагностике следует иметь в виду алейкемический ретикулез, эритролейкоз (синдром ди Гульельмо), болезнь Верльгофа и гемолитическую анемию с преимущественным внутрисосудистым гемолизом (болезнь Маркиафава- Микели). В пользу алейкемического ретикулеза говорят такие симптомы, как общая резкая интоксикация, повышение температуры, боли в костях, увеличение в ряде случаев периферических лимфатических узлов, а нередко и селезенки. При ретикулезе на фоне панцитопении в гемограмме могут наблюдаться недифференцированные элементы. Трепанобиопсия более, чем пунктат костного мозга, помогает уточнить диагноз.
При апластической (гипопластической) анемии костный мозг беден костномозговыми элементами. Полости его по преимуществу заполнены жировыми клетками. При алейкемическом ретикулезе отмечаются рассасывание кости и гиперплазия ретикулярных элементов. В дифференциальном диагнозе с болезнью Верльгофа имеют значение следующие моменты. При болезни Верльгофа степень анемии адекватна степени кровопотери. В костном мозгу определяется повышенное количество функционально неполноценных мегакариоцитов без отшнуровки тромбоцитов. При гипоплазии кроветворения анемия часто предшествует геморрагическому диатезу. В костном мозгу — малое количество мегакариоцитов. В отличие от гипопластической анемии эритролейкоз сопровождается признаками гемолиза (выходе кровяное русло эритро — и нормобластов, повышенное количество ретикулоцитов), появлением в крови гемоцитобластов. В костном мозгу при этом синдроме увеличивается число недифференцированных клеток, встречаются мегалобластоидные эритробласты, нередко наблюдается увеличение селезенки.
Лечение ахрестической анемии симптоматическое и направлено на борьбу с анемическим синдромом и геморрагиями, а также на стимуляцию кроветворной функции костного мозга. Переливание свежезаготовленной крови или эритроцитной массы по 250 или 125 мл с короткими перерывами. Витамины группы В как регуляторы и стимуляторы гемопоэза: подкожно ежедневно по 2 мл 5% раствора витамина B1, внутрь по 5 мг витамина В2 3 раза в день, внутримышечно по 50 мг витамина В6 ежедневно и по 100 мкг витамина B12 через день; никотиновая и фолиевая кислоты по 30 мг 3 раза в день внутрь.
Кортикостероидные гормоны, стимулирующие миелоидное кроветворение, показаны особенно при наличии геморрагического синдрома или накоплении в крови аутоантител. Назначают преднизон по 40-50 мг в сутки в течение 2-3 недель с последующим переходом на поддерживающие дозы 20-15 мг в день. С целью стимуляции гемопоэза в комплекс лечебных мероприятий назначают также анаболические гормоны, в частности неробол по 5 мг 4-6 раз в день.
В случае неэффективности консервативной терапии рекомендуется спленэктомия при гипопластических формах в период, более или менее свободный от геморрагических проявлений, с целью снятия тормозящего влияния селезенки на костномозговое кроветворение.
В связи с наблюдениями о вовлечении селезенки в патологический процесс при гипоплазии кроветворения уже в самом начале заболевания встает вопрос о возможности производства операции удаления селезенки в раннем периоде заболевания.
Переливание костного мозга (с тщательным серологическим подбором донора), производимое однократно или повторно, способствует повышению числа ремиссий.
Агранулоцитоз
Агранулоцитоз представляет собой клинико-гематологический синдром, в основе которого лежит изолированное поражение гранулопоэза. При этом синдроме наблюдается резкое снижение гранулоцитов вплоть до полного их исчезновения.
Этиология агранулоцитоза. К известным факторам относятся агенты инфекционные (при сепсисе, воспалении легких, брюшном тифе и пр.), медикаментозные (хинин, барбитураты, мышьяк, метилтиоурацил, амидопирин, сульфаниламиды, стрептомицин, ПАСК и др.), лучевые (рентгеновы лучи, радий, радиоизотопы). Агранулоцитоз инфекционного и особенно медикаментозного происхождения встречается наиболее часто.
В развитии агранулоцитоза играет роль реактивное состояние организма.
Симптомы, течение агранулоцитоза. Начало заболевания, как правило, внезапное. Язвенно-некротическая ангина сопровождается высокой лихорадкой интермиттирующего типа с симптомами тяжелой общей интоксикации. Часто сопутствуют симптомы проявления аллергизации в виде herpes labialis et nasalis, протекающих с некрозами. Наблюдается развитие некроза и в других областях тела (в гортани, по ходу кишечника, в области половых органов, промежности, анального отверстия и пр.). В некоторых случаях заболевание осложняется пневмонией, склонной к абсцедированию. Нередко наблюдается увеличение подчелюстных, шейных, а иногда и подмышечных лимфатических узлов, увеличение селезенки.
Картина крови характеризуется резкой лейкопенией (до 1000 лейкоцитов и меньше в 1 мм3 крови), нейтропенией (вплоть до полного исчезновения гранулоцитов) и относительным лимфоцитозом. Отмечается снижение числа эозинофилов, увеличение плазматических клеток.
Миелограмма характеризуется нерезким уменьшением общего количества миелокариоцитов с нарушением созревания гранулоцитов, уменьшением их числа и увеличением процента незрелых форм. Количество лимфоидных клеток несколько увеличено.
После выздоровления у большинства больных остается лабильность (неустойчивость) лейкопоэза, особенно выраженная после перенесения инфекции (грипп, катар верхних дыхательных путей и пр.), возникает наклонность к рецидивированию заболевания.
В таких случаях развиваются формы рецидивирующего агранулоцитоза или состояние хронической гипогранулоцитарной реакции.
Распознавание агранулоцитоза. не представляет затруднений. Трудно дифференцировать от острого алейкемического ретикулеза, характеризующегося лейкопенией. Решающим диагностическим критерием в пользу ретикулеза служит гиперплазия костномозговых клеток за счет недифференцированных элементов. В случаях же алейкемического ретикулеза, когда при пункции костного мозга не удается получить пунктат или он бывает чрезвычайно беден клеточными элементами и не раскрывает истинной природы заболевания, следует применять трепанобиопсию. Картина рассасывания кости с ретикулярной гиперплазией, характерная для ретикулеза, позволяет дифференцировать его от агранулоцитоза.
Лечение агранулоцитоза. Устранение причины заболевания, если удается ее выявить, применение средств, стимулирующих гемопоэз и лейкопоэз, назначение симптоматической терапии по борьбе с инфекцией.
При тяжелом течении лечение следует начинать с повторных переливаний свежезаготовленной крови или эритроцитной массы.
С целью стимуляции гемопоэза рекомендуется назначение кортикостероидных гормонов (преднизолон по 0,05-0,06 г в сутки, кортизон по 0,15-0,2 г в сутки) витаминов группы В, лейкогена по 0,02 г 3 раза в день, пентоксила по 0,2-0,3 г 3 раза в день, 5% раствора нуклеиновокислого натрия по 5-10 мл внутримышечно ежедневно.
С самого начала лечения больным необходимы антибиотики широкого спектра действия, десенсибилизирующие средства (димедрол по 0,05 г 3 раза в день, глюконат кальция по 0,5 г 3 раза в день или 10% раствор хлорида кальция по 1 столовой ложке 3 раза в день, супрастин по 0,025 г 3 раза в день), туалет полости рта.
http://medikweb.ru/spravochnik_vracha/glava1/aplasticheskie-i-gipoplasticheskie-anemii.php
Гипопластическая и апластическая анемия

Гипопластическая и апластическая анемия – Anaemia hipoplastica et aplastica –называются остро протекающие заболевания системы крови, развивающееся в результате недостаточности (истощения) костномозгового кроветворения и проявляющиеся нормоцитарной, иногда макроцитарной, нормохромной анемией с сопутствующей тромбо- и гранулоцитопенией (панцитопенией).
Этиология. Причины дефицитных анемий – алиментарные факторы: недостаток в рационе кормления животных протеина , отдельных аминокислот, микроэлементов (железа, меди, кобальта), витаминов (В12, А, Д, С и других). Гипопластические анемии могут служить симптомами хронических гастро-энтероколитов, гепатитов, дистрофий печени, обусловленных пониженной усвояемостью питательных веществ (даже при полноценном кормление животных). Миелотоксические анемии у животных возникают в результате инфекций, инвазий и интоксикаций, чаще при хроническом течении (туберкулез, паратуберкулез, лептоспироз, листериоз, диктиокаулез, аскаридоз, мониезиоз, микозы, кетозы, эндометриты и др.). Анапластические анемии являются следствием воздействия на организм животного в больших дозах ионизирующей радиации (лучевая болезнь), отравления бензолом, соединениями свинца, ртути и других тяжелых интоксикациях.
Патогенез изучен слабо. Под влиянием вышеуказанных этиологических факторов у больного животного вначале развивается гипоплазия, а затем наступает аплазия костного мозга, если доза того или иного фактора достаточно долговременная. Причинные факторы, подавляющие костно — мозговое кроветворение, не вызывают разрушения эритроцитов, анемия развивается в основном за счет уменьшения их регенерации, да и не только их, а и всех клеточных элементов костного мозга. Поэтому наряду с развитием анемии отмечается лейкопения и тромбопения. Происходит одновременно повышение ломкости и порозности кровеносных сосудов, в результате у больного животного появляются кровоизлияния. В последующем пониженная фагоцитарная активность элементов соединительной ткани на фоне лейкопении и резко сниженной способности выработки антител ведет к развитию у животного бактериемии и сепсису.
Патологоанатомические изменения. Слизистые и серозные оболочки у павших животных бледные, часто с точечными и полосчатыми кровоизлияниями. В селезенке кровоизлияния. В легких, иногда в печени, почках и желудочно – кишечном тракте застойная гиперемия. В паренхиматозных органах и коже нередко устанавливаем некрозы. Костный мозг, особенно в трубчатых костях — бледный, местами желтый – жировой. В миокарде, печени и почках выраженная дистрофия.
Клинические признаки. На фоне основного заболевания (инфекция, инвазия, отравление) при гипопластической анемии у больного животного прогрессирует общая слабость, быстрая утомляемость, угнетение, отмечаем снижение продуктивности и работоспособности, появляются симптомы расстройства желудочно- кишечного тракта, сухость и взъерошенность кожного покрова, понижается эластичность кожи. При клиническом исследование больного животного устанавливаем характерный признак болезни — бледность видимых слизистых оболочек, склеры и кожи. При апластической анемии в сильной степени выражены общая слабость (иногда больные животные не в состоянии стоять на ногах), животные апатичные, при клиническом осмотре отмечаем бледность видимых слизистых оболочек и кровоизлияния на слизистых оболочках и коже.
Наряду с развитием у больного животного анемии отмечаем быстрое снижение количества лейкоцитов в крови и клеточных элементов в костном мозге. Количество гранулоцитов крови, молодых эритробластических форм и гранулофилоцитов в костном мозге снижается до минимума.
В лейкоцитарной формуле происходит нарастание процента нейтрофилов, а в миелограмме – миелобластических форм. При стахиоботриотоксикозе, чуме количество лейкоцитов крови снижается до 500-100 в 1мм?, резко выражен относительный лимфоцитоз, нейтропения, эозинофилы и моноциты исчезают, нарастает тромбопения. СОЭ ускорена. В костном мозге миелоидные элементы подвергаются дегенеративным изменениям. При тяжелом течении апластической анемии костный мозг становится опустошенным – отмечается бледность клеточными элементами костного мозга (панмиелофтиз). При исследовании обнаруживают в основном только гистиоцитарные и плазматические клетки, и единичные эритробластические формы.
В результате уменьшения массы кроветворной ткани эритропоэз становится явно недостаточным для поддержания состава крови на необходимом уровне; анемия прогрессирует, ее характер может отклонится в сторону гиперхромии. Гемоглобинизация эритроблостав совершается по типу эмбрионального эритропоэза; исчезновение ядра из клетки замедленно и совершается только путем кариорексиса.
Течение чаще острое и отличается своей злокачественностью. На фоне аплазии кроветворной ткани в организме развиваются вторичные инфекции, очаги некрозов, кровотечения и сепсис. Но бывают случаи медленного течения, причем патологические симптомы анемии постепенно усиливаются.
Диагноз на апластическую анемию ставится с учетом анамнеза (интоксикация, инфекция, инвазия), клинических симптомов (анемия, слабость) и анализа крови. Гематологически при гипо- и апластических анемиях устанавливают понижение уровня гемоглобина, лейкопению с преобладанием зрелых форм нейтрофилов, повешенную СОЭ. Характерной особенностью этих групп анемий в отличие от постгеморрагических и гемолитических является пониженное содержание в каждом эритроците гемоглобина при незначительном уменьшении в крови количества эритроцитов, что обуславливает низкий цветовой показатель (обычно хромных) эритроцитов, измененных патологических форм и размеров: пойкилоцитоз, анизоцитоз, большое количество микроцитов (малых размеров по сравнению с нормой), встречаются анулоциты (в виде колец), шизоцыты (в виде обрывков) и др. При исследовании пунктата костного мозга обнаруживают бледность клеточными элементами всех ростков, кровоизлияния.
Дифференциальный диагноз. Заболевание необходимо дифференцировать от гипопластических анемий, анемий при лейкозах у животных, лучевой болезни, ИНАН лошадей, чумы свиней.
Лечение. Прежде чем приступить к лечению, необходимо устранить этиологические факторы вызвавшие заболевание и угнетающие кроветворение. При наличии у больного животного тех или иных инвазионных, инфекционных заболеваний и отравлений необходимо проводить соответствующее лечение при данных заболеваниях. Больных животных обеспечивают полноценным рационом кормления с достаточным количеством содержания протеина, полным набором аминокислот, витаминов, макро- и микроэлементов. Для стимулирования костно- мозгового кроветворения необходимо применять препараты железа, кобальта, меди, мышьяка, кампонол, витамины К, В12, фолиевую кислоту и другие. Хорошее лечебное действие оказывает переливание гомогенной стабилизированной крови, внутримышечные или подкожные введения гомогенной или гетерогенной крови, гамма — и полиглобулинов согласно инструкциям и в дозах исходя из наставления по их применению.
При нарастающих симптомах интоксикации при комплексном лечении применяют сердечные средства, 20-40% раствор глюкозы с аскорбиновой кислотой.
При септических осложнениях применяют антибиотики, в том числе современные цефалоспоринового ряда. При полном истощении костного мозга лечить больное животное не целесообразно.
http://vetvo.ru/gipoplasticheskaya-i-aplasticheskaya-anemiya.html