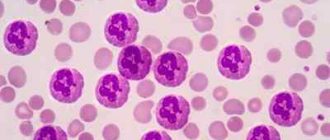
Легочная гипертензия новорожденных — причины, симптомы, диагностика и лечение
Легочная гипертензия новорожденных

Легочная гипертензия новорожденных – состояние рефрактерного повышения сосудистого сопротивления в легких и шунтирования крови в обход малого круга кровообращения с развитием гипоксемии. Основными проявлениями являются стойкий центральный цианоз, учащение дыхания и положительная реакция на кислородотерапию. Диагностируется с помощью определения газового состава крови, а также на ЭКГ и ЭхоКГ, которые подтверждают гипертрофию правых отделов сердца и факт шунтирования крови в обход легких. Лечение комплексное, направлено на расширение сосудов легких с целью нормализации оксигенации, поддержание артериального давления, коррекцию водно-электролитного баланса и др.
Легочная гипертензия новорожденных
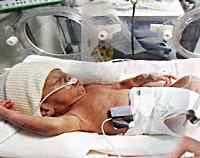
Легочная гипертензия новорожденных – достаточно распространенное патологическое состояние. В норме легочная гипертензия присутствует до рождения. С началом легочного дыхания давление в сосудах легких должно снизиться, чего в данном случае по различным причинам не происходит. Частота заболевания – 1-6 случаев на 1000 новорожденных, дети обычно доношенные. Актуальность легочной гипертензии новорожденных в педиатрии связана достаточно высокой смертностью (10-20% случаев), которая лишь незначительно снижается по мере развития современных медицинских технологий. Высоким остается также процент инвалидизации вследствие длительной гипоксемии и продолжительной искусственной оксигенации. Растет количество форм заболевания, связанных с генетическими синдромами, и в целом число ассоциированных форм, что осложняет терапию.
Причины и классификация легочной гипертензии новорожденных
В большинстве случаев легочная гипертензия новорожденных является следствием дефекта адаптации сосудов легких к изменению концентрации кислорода после рождения. Способствовать высокому сосудистому давлению в легких могут многие факторы, например, внутриутробные инфекции плода, прием матерью различных препаратов во время беременности, гипоксия в родах и др. Кроме того, причиной развития заболевания нередко становятся синдром аспирации мекония, респираторный дистресс-синдром и пневмония. Легочная гипертензия новорожденных регистрируется при гипоплазии легких и диафрагмальных грыжах. Оба этих состояния ведут к снижению общей площади альвеол и легочных капилляров, что вызывает повышение сосудистого давления.
Согласно современной классификации, принятой Институтом изучения заболеваний сосудов легких в 2011 году, выделяют две основные группы легочной гипертензии новорожденных: врожденную и персистирующую. Врожденная легочная гипертензия новорожденных может быть связана:
- С материнскими причинами (хориоамнионит, преэклампсия и др.).
- С нарушением развития легочных сосудов ребенка (гипоплазия легких, диафрагмальные грыжи, альвеолярная дисплазия, аномалии легочных сосудов).
- С врожденными пороками сердечно-сосудистой системы (преждевременное закрытие овального окна или артериального протока и др.).
Персистирующая легочная гипертензия новорожденных обусловлена стойким дефектом адаптации легочных сосудов и может быть идиопатической (когда причина неизвестна), либо связанной с синдромом аспирации мекония, сепсисом, пневмонией, приемом некоторых лекарственных препаратов и другими обстоятельствами.
Симптомы и диагностика легочной гипертензии новорожденных
В 77% случаев заболевание развивается в первые сутки жизни малыша. Основным проявлением легочной гипертензии новорожденных является стойкий центральный цианоз, который, как правило, не соответствует степени выраженности патологических изменений в легких. Дыхание ребенка учащено, но не критически. Артериальное давление чаще в норме, по мере развития состояния постепенно снижается. Патогномоничным признаком считается разница оксигенации в большом и малом кругах кровообращения от 20% и выше. Определить это можно, одновременно измерив парциальное давление кислорода в большом и малом круге кровообращения. Также при легочной гипертензии новорожденных отмечается положительная реакция на кислородотерапию. Кроме цианоза и тахипноэ в ряде случаев обнаруживаются симптомы аспирации мекония, пневмонии и других заболеваний, которые могут вызвать повышение сопротивления в легочных сосудах.
Первичный физикальный осмотр педиатра позволяет выявить цианоз кожных покровов. Аускультативные изменения в легких выражены, как правило, незначительно. При аускультации сердца характерным является систолический щелчок над легочной артерией и акцент второго тона там же. Легочная гипертензия новорожденных подтверждается лабораторными методами диагностики. Общий и биохимический анализ крови обнаруживают полицитемию, гипокальциемию и гипогликемию. Гипоксемия определяется анализом газов крови. Рентгенограмма легких чаще в норме, кроме случаев пневмонии. ЭКГ и ЭхоКГ свидетельствуют о гипертрофии правых отделов сердца, которым при легочной гипертензии новорожденных приходится работать фактически на оба круга кровообращения.
Патологию помогают диагностировать гипероксические тесты, позволяющие достоверно определить наличие сброса крови через открытые эмбриональные отверстия (артериальный проток, овальное окно) из малого круга кровообращения в большой, минуя легкие. Для детей, находящихся на искусственной вентиляции легких, возможно проведение гипервентиляционного гипероксического теста. Для этого частоту дыхания повышают до 80-100 в минуту на 5-10 минут. Диагноз легочной гипертензии новорожденных подтверждается, если цианоз исчезает. Если же цианоз остается, можно заподозрить у ребенка порок сердца «синего типа».
Лечение и прогноз при легочной гипертензии новорожденных
Терапия направлена на снижение сосудистого сопротивления в легких и лечение сопутствующего заболевания. Показан строгий лечебно-охранительный режим, количество манипуляций с ребенком стараются свести к необходимому минимуму. Как правило, речь идет о кювезном режиме в палате интенсивной терапии или реанимации. Независимо от причины легочной гипертензии новорожденных, лечение начинают с введения обезболивающих и седативных препаратов. Это позволяет минимизировать нагрузку на легкие и сердце.
Проводят инфузионную терапию с целью поддержания адекватного сердечного выброса и концентрации электролитов. Для поддержания артериального давления показаны инотропные препараты. Коррекцию гипоксемии осуществляют с использованием кислородотерапии, методом выбора в первые 2-3 суток является конвекционная ИВЛ. Для нормализации сосудистого давления в легких применяют вазодилататоры, которые могут назначаться ингаляционно в составе дыхательной смеси для ИВЛ, вводиться внутривенно или перорально. С этой же целью используют простагландины. В тяжелых случаях требуется экстракорпоральная мембранная оксигенация крови.
Осуществляют терапию основного заболевания, при патологии инфекционного генеза показаны антибиотики. Даже без подтвержденной пневмонии или сепсиса антибиотикотерапию часто назначают превентивно. В случае гипоплазии легких, диафрагмальной грыжи или подтвержденных врожденных пороков сердца и легких необходимо оперативное лечение. Методику выбирают в зависимости от типа патологии, в отдельных случаях выполняют пересадку легких или комплекса «легкие-сердце».
Прогноз легочной гипертензии новорожденных неблагоприятный. Кроме высокой смертности, о которой было сказано выше, примерно 25% выживших детей в дальнейшем имеют признаки отставания в физическом и умственном развитии. Часто возникают хронические легочные заболевания и нейросенсорные расстройства слуха. Профилактики заболевания не существует.
http://www.krasotaimedicina.ru/diseases/children/neonatal-pulmonary-hypertension
Лёгочная гипертензия у детей
Лёгочная гипертензия – явление, сопровождающееся повышением кровяного давления в лёгочной артерии. Такое состояние провоцирует постепенное сужение сосудов в лёгких с последующим исчезновением просвета. Особенности развития и течения заболевания зависят от его формы и первичных причин возникновения.
Лёгочная гипертензия представлена двумя формами заболевания: первичной и вторичной. Такая особенность связана с причинами развития болезни в организме ребёнка, а также протеканием заболевания.
Первичная лёгочная гипертензия характеризуется как заболевание неизвестной этиологии. Причины, что может вызвать патологию такого типа, изучаются медиками до сих пор. Однако было отмечено, что такая форма заболевания не имеет связи с другими нарушениями в работе органов дыхания и сердечно-сосудистой системы. Большое значение придаётся наследственному фактору.
Особенности того, как развивается и проявляется вторичная лёгочная гипертензия, определённым образом отличаются. Факторы, от чего может быть патология данного рода у ребёнка, включают в себя:
- токсическое воздействие на органы дыхания,
- деструктивную пневмонию,
- бронхиальную астму,
- воспалительные процессы в лёгких с последующим разрушением бронхов.
Гипертензия лёгких может возникать у новорождённых детей. В таком случае заболевание развивается на фоне патологий в органах дыхания, появившихся в период вынашивания плода.
Лёгочная гипертензия у детей начинает проявляться не сразу. Вторичная форма развивается медленно, на фоне других заболеваний, поэтому первые признаки патологии могут проявить себя через некоторое время. К характерным симптомам относятся:
- частая одышка, которая возникает при минимальной физической нагрузке и сохраняется в состоянии покоя;
- учащённое сердцебиение, что возникает вследствие нехватки кислорода в крови;
- сдавливающие болезненные ощущения в спине;
- возможна потеря сознания при физических нагрузках;
- необоснованная и неконтролируемая потеря массы тела ребёнка;
- ощущение дискомфорта в животе, возможна тошнота, характерные боли;
- плохое настроение, подавленность и повышенная утомляемость;
- снижение активности ребёнка;
- появление сухого кашля, охриплость голоса.
Со временем признаки заболевания могут ухудшаться. Так, например, при осложнённой форме гипертензии лёгких возможен кашель с кровью. Такое проявление свидетельствует о прогрессирующей отёчности лёгких.
Диагностика лёгочной гипертензии у ребёнка
Если родители смогли распознать характерные симптомы, ребёнка следует показать специалисту. Диагностировать заболевание и определить его форму помогут специальные процедуры:
- осмотр маленького пациента и составление анамнеза с целью определить приблизительное время, когда начали проявляться первые симптомы;
- изучение истории болезни для выяснения обстоятельств и причин, что могло вызвать развитие патологии;
- проведение электрокардиограммы для составления характеристики работы сердца;
- ультразвуковое исследование сердца для определения размеров органа и измерения давления в лёгочной артерии;
- катетеризация лёгочной артерии для уточнения диагноза, определения степени тяжести состояния;
- проведение специальных анализов для выяснения показателей здоровья ребёнка.
Для определения диагноза и назначения курса лечения ребёнку необходимо посетить врачей:
- педиатра,
- детского пульмонолога,
- кардиолога.
Осложнения
Нарушение структуры и функционирования сосудов может спровоцировать недостаток кислорода в организме ребёнка. Такое состояние угрожает не только гармоничному росту и развитию, но и жизни маленького пациента.
Возможны и другие осложнения, чем опасна лёгочная гипертензия для ребёнка:
- развитие сердечной недостаточности,
- возникновение тромбов в сосудах лёгких,
- изменение ритма сердца,
- отёк лёгких.
При отсутствии своевременной терапии такие осложнения способны изменить качество жизни ребёнка в будущем.
Что можете сделать вы
Чтобы вылечить лёгочную гипертензию у ребёнка, необходимо точно установить причину развития патологии. Курс лечения направлен на:
- устранение основного заболевания (при вторичной гипертензии лёгких у ребенка);
- снижение давления в артерии;
- нормализацию уровня кислорода в крови;
- предупреждение гипоксии;
- профилактику осложнений.
Задача родителей состоит в постоянном контроле состояния здоровья ребёнка и выполнении всех назначенных лечебных мер. Протекание болезни можно облегчить с помощью применения специальной терапии. Главное, что нужно для этого делать, – это:
- соблюдать приём медикаментов, назначенных лечащим врачом;
- проводить массажи и выполнять упражнения в соответствии с лечебной физкультурой;
- посещать санатории для укрепления общего состояния организма и улучшения состояния ребёнка.
Также вам необходимо регулярно водить ребёнка на приёмы к лечащему врачу для стационарного наблюдения состояния здоровья.
Что делает врач
В зависимости от состояния здоровья ребёнка и степени тяжести лёгочной гипертензии специалист может назначить:
- приём медикаментов для стабилизации давления в артерии и предупреждения гипоксии;
- госпитализацию пациента для наблюдения в стационарном режиме;
- проведение операции в случае, если лечить ребёнка другими методами не удаётся.
В редких случаях может понадобиться трансплантация лёгкого.
Профилактика
Специфика развития и течения первичной формы заболевания значительно снижает эффективность проведения каких-либо профилактических мер. В случае с вторичной лёгочной гипертензией предотвратить появление патологических процессов вполне возможно. Для этого необходимо:
- осуществлять своевременное лечение и контролировать состояние здоровья ребёнка, у которого диагностировали бронхолёгочные заболевания;
- приучать ребёнка к здоровому образу жизни;
- исключить вредные привычки (курение) у подростков;
- приучать ребёнка к регулярной физической активности (неинтенсивной): длительным прогулкам, утренним зарядкам, особенно на свежем воздухе; стараться избегать стрессовых ситуаций.
http://detstrana.ru/service/disease/children/lyogochnaya-gipertenziya/
Легочная гипертензия в детском и юношеском возрасте (часть 2)
Клинические проявления и диагностика
Первыми клиническими признаками первичной или вторичной РН часто являются диспное при нагрузке или синкопе. Оба симптома являются следствием ограниченной способности увеличивать, в условиях покоя еще нормальный сердечный выброс, а вместе с тем поступление кислорода на периферию при физической нагрузке. При этом синкопе является результатом сниженного церебрального кровотока, который еще больше уменьшается в результате индуцированной физической нагрузкой периферической вазодилатации. Некоторые дети в отношении церебральных приступов получают неправильное лечение.
Маленькие дети в ретроспективном анализе часто обращают на себя внимание появлением возрастающей усталости или интуитивным отказом от повседневности. За исключением детей с известным семейным РРН, эта неспецифичная первичная симптоматика оказывается причиной чаще всего отсроченной постановки диагноза, особенно в детском возрасте, при этом часто с отсрочкой на 2-4 года.
Также типичным является ошибочный диагноз обструктивного заболевания легких вплоть до бронхиальной астмы, так как почти у всех пациентов со значительной легочной гипертензией в зависимости от степени тяжести заболевания сосудов легких развивается сопутствующая обструкция бронхов.
Пациенты более старшего возраста часто жалуются на головные боли и пектангиозные боли. Последние возникают в результате ишемии правого желудочка вследствие ограниченного коронарного кровотока при возросшей мышечной массе правого желудочка и повышенного энддиастолического и систолического давлений в правом желудочке. Периферические отеки, как следствие недостаточности правого сердца, являются выражением далеко зашедшего заболевания. Цианоз в покое при РРН является, за исключением пациентов с интракардиальными или аортопульмональными коммуникациями, следствием сниженного смешанного венозного насыщения кислородом (SvO2). При этом цианоз оказывается поздним симптомом или даже выражением другого основного заболевания или дополнительно приобретенного заболевания паренхимы легких. Сниженные значения SvO2 часто коррелируют с повышенным пульмонально капиллярным давлением вследствие обусловленной правожелудочковой дилатацией наруше-нием диастолической функции левого желудочка. После постановки диагноза ожидаемая продолжительность жизни у детей оказывается короче, чем у взрослых пациентов. У взрослых с РРН и значениями SvO2 2+
2.Скрининг на тромбофилию
Профиль свертывания с
Факультативно \»tissue factor\»
3. Специальные исследвоания
Аргинин и цитрулин в плазме
Тест функции щитовидной железы
Функциональные тесты печени
Профиль липидов включая Lpa
Скрининг на инфекцию включая ВИЧ
CH50-комплемента и
компоненетов комплемента
Типирование -HLAУровень в сыворотке АСЕ
На ЭКГ опрделяются признаки правожелудочковой гипертрофии с нарушениями реполяризации. Корреляция с пульмонально-артериальной высотой давления обычно отсутствует. р-декстрокардиальный признак скорее является поздним признаком. Для установления нарушений ритма необходим 24-часой Holter-ЭКГ. При подозрении на пектангиозные боли (боли в груди!), в случае если позволяет возраст показано проведение ЭКГ с нагрузкой.
На рентгенограмме в >90% случаев выявляется признаки РН. Размеры сердца при компенсированном состоянии РН пока еще нормальны. Характерным является выдающийся pulmonalis сегмент и расширенные сосуды Hilus с ясной периферией легких, которые соответствуют обрывам сосудов. При остром обострении обнаруживается кардиомегалия и отек легких.
Эхокардиография позволяет исключить посткапиллярный РН вследствие сердечной недостаточности, заболевания митрального клапана или другого врожденного порока сердца. Она делает возможным постановку точного диагноза на основании морфологических и функциональных характеристик значительного (Р)РН. При этом правое предсердие и желудочек увеличены. Полость левого желудочка нормальна или уменьшена и действует ограничено. На 2D-Echo межжелудочковая конфигурация перегородки, правожелудочковые пристеночные силы и ширина правожелудочкового тракта оттока или, по обстоятельствам, ствол пульмональной артерии указывают на величину правожелудочковой гипертензии.
Систолическая и диастолическая девиация перегородки влево с ограничением размера полости левого желудочка и обратное соотношение E/A доплерсонографического митрального втока коррелируют с супрасистемным давлением в правом желудочке, с чрезмерно дилатированной полостью и связанным с этим диастолическим нарушением функции левого желудочка.
У детей более старшего возраста и взрослых изменяющаяся с сердечным циклом ширина нижней полой вены есть опосредованное указание на давление в правом предсердии. Если V.cava inferior расширена и присутствует утрата фазового изменения ширины, то нужно исходить из величины центрального венозного давления >15 mmHg. При клиническом симптоме цианоза следует провести дифференциально диагностическую оценку справо-налево шунта на уровне предсердий. Обычно выявление или исключение открытого Foremen ovale имеет прогностическое значение, и у подростков, и взрослых лучше всего устанавливается с помощью трансэзофагальной эхокардиографии. Она также является методом выбора для исключения или выяв-ления внутрикардиальных тромбов.
Пульмональное артериальное давление полуколичественно определяется методами M-Mode, 2D-отображения, систолических временных интервалов или допплеровской техникой. О недостаточности трикуспидального клапана может говорить давление в правом желудочке, а при отсутствии правовентрикулярной обструкции можно сделать заключение о систолическом пульмональном давлении.
Если имеется недостаточность пульмонального клапана, можно оценить диастолическое пульмональное давление. При знании кровяного давления измерение систоли-ческой скорости через посттрикуспидальную коммуникацию при шунтовых пороках позволяет оценить уровень давления правого сердца. Имеется корреляция также между средним пульмонально-артериальным давлением и временем ускорения в правожелудочковом тракте оттока измеренной скорости, при чем разброс значений в отдельных случаях не позволяет сделать никаких уверенных суждений.
Перфузионная сцинциография необходима не только для исключения тромбоэмболической пульмональной гипертензии, но также в общем для исключения нарушения соотношения вентиляция/перфузия при РРН. Ангиографически не распознаваемые региональные выпады перфузии поддерживают показание к проведению антикоагуляции. В отдельных случаях рациональной оказывается и вентиляционная сцинциография.
Магниторезонанасная томография или диагностика с помощью высокоразрешающей компьютерной томографии выдвигаются на первый план при исключении или подтверждения тромбоэмболической РН или аномалии пульмональной вены в отношении диагностической пульмональартериографией. Кроме того, возможен подсчет сердечного объема с определением соотношений величин камер сердца.
Биопсия легких требуется лишь факультативно (например, при интестинальном гемангиомутзе).
Исследование с помощью катетеризации сердца безусловно необходимы для точной диагностики РРН, пороков сердца с РН или при наличии симптоматической РН, несмотря на последовательное лечение основного заболевания. При центральной тромбоэмболизации с помощью катетерной интеррвенции возможно проведение не только неотложной терапии фрагментации тромба методом Pigtail, Clotbuster или локального тромболиза, но и при хронической форме также и баллонной дилатации тромбозированного участка сосуда в качестве альтернативы хирургической пульмональной тромбоэктомии в отдельных случаях.
Региональная (wedge) ангиография рекомендуется для визуальной оценки легочного сосудистого древа и во избежании индуцированных большим количеством контрастного вещества пульмонально-артериальных кризов.
Гемодинамическая оценка должна, когда это возможно, проводится при спонтанном дыхании, но при интубационной готовности. Необходима не только подготовленность к проведению интубации, но должны быть соблюдены и соответствующие высшей степени всеохватывающие условия безопасности и в основе должна сохраняться реанимационная готовность, когда у пациента с РН в условиях катетеризации остро разовьется декомпенсация. По собственному опыту детей и подростков можно обследовать при проведении начального седирования диазепамом 0,2-0,5 mg/kg i.v. как ED, а при пункции сосудов проводить повторную анальгезию кетамином 0,2-0,5 mg/kg i.v. сопровождающейся продолжительной инфузией пропофолом 1-2 mg/kg час. При этом анальго-седировании, как правило, сохраняется достаточное спонтанное дыхание (paCO2 35-45 mmHg). У пациентов более старшего возрасте способных к кооперации для ло-кальной анестезии и установки катетера чаще всего в качестве ED бывает необходим только мидазолам 0,1-0,2 mg/kg i.v. Важно отметить, что никакой премедикации в отсутствие врача проводится не должно.
В рамках диагностики или исключения врожденного порока сердца или вообще посткапиллярной пульмональной гипертензии необходимо провести измерение пульмоартериального \»wedge\» — и/или левоатриального давления.
Для необходимой проверки Reagibilitat пульмональных сосудов предпочтение отдается введению через бедренную вену катетера или 5F-проводника, с помощью которого одновременно устанавливается 0,014-дюймовая двойная проволока в левой головке нижней доли — или сегмен-та. При шунтовых пороках \»дополнительно\» через вторую вену в V.cava superior устанавливается 4F-\»multipurpose\» (многоцелевой) катетер. Артериальное давление измеряется с помощью применяемого для катетеризации сердца или собственно установленного 3F-артериального катетера. При этом одновременно можно проводить интравазальные измерения кровяного дав-ления и анализ газов крови, а также продолжительное измерение региональных пульмональных кровотоков. Расчеты объема сердечного выброса за единицу времени по принципу Fick и вместе с тем также пульмонального (Rp) и системного (Rs) сосудистого сопротивления, включая соотношение Rp/Rs, проводится по стандартным формулам. Потребление кислорода при этом измеряется напрямую или берется из стандартизированных таблиц.
Сохраняющаяся Reagibilitat сосудов легких на вазодилататоры коррелирует с продолжительностью выживания пациентов. Реакция на острое тестирование одним из диалататоров также предиктивна в отношении реагирования на оральное, ингалятивное или i.v. продолжительное лечение. Для минимизации риска это проводится с вазодилататорами короткого действия, внутривенными и ингаляционно применяемыми вазодилататорами.
Эффективность определяется по снижению пульмонально-артериального давления и сопротивления сосудов. Решающим однако является снижение соотношения пульмонального к системному давлению крови и/или сопротивления сосудов. При использовании отношения Rp/Rs в качестве коэфициента решается проблема возможного необходимого расчета потребления кислорода. Согласно определению имеет место эффективная пульмональная вазодилатация, когда сопротивление сосудов легких снижается на более, чем 20% , а пульмонально-артериальное давление у пациентов без выравнивающих давление шунтовых пороков на более, чем 10% от исходного значения. При медикаментозной проверке следует обращать внимание на то, что могут происходить спонтанные, находящееся в области критериев эффективности, \»колебания\» пульмонально-артериального давления.
Преоперативное обследование сердечного порока с РН касается вопроса операбельности. Дети с врожденным пороком сердца и нарушенной пульмонально-васкулярной структурой и функцией имеют повышенный риск, связанный с оперативным вмешательством. Применение экстракорпоральной циркуляции приводит к дополнительным ишемическим реперфузионным повреждениям эндотелия сосудов легких с риском развития пульмональных сосудистых спазмов. Поэтому рационально, уже преоперативно определить профиль зависимых и не зависимых от эндотелия пульмональных вазодилатаций.
Пациенты с шунтовыми пороками, у которых сопротивление легочных сосудов при тестировании ингаляционными вазодилататорами (кислород, FiO2 0,8-0,9 в комбинации, например, с NO до 40 ppm или илопростом 0,2-1,5 mg/kg разведенным 2-5 ml NaCl 0,9%) не может снизиться ниже 9-10 единиц Wood или достичь соотношения Rp/Rs 0,8 отмечается, согласно критериям определения, Reagibilitat сосудистого ложа легких, то никаких дальнейших медикаментозных тестов на Reagibilitat не требуется.
Применение простациклина, аналогов простациклина или монооксида азота (NO) проводится при неоднозначном эффекте на кислород или для установления дозы вазодилатационной продолжительной терапии.
Тестирование с ингаляционным монооксидом азота (NO) до максимальной концентрации 40 ppm оправдано тогда, когда на повышение инспирированной фракции кислорода (FiO2 0,8-1) не отмечается никакой пульмональной сосудистой реакции. В рамках работы компетентной сети \»Врожденные пороки\» предусмотрено тестирование с NO до Wppm. Проведенение осуществляется с помощью IN-Ovent delivery System. Доза в 5 ppm NO соответствует пульмональнова-зодилатирующему действию ингаляции 100% кислородом. Релаксация сосудов при NO происходит путем активации растворимой гианилатциклазы. Это энзим конвертирует гуано-зинтрифосфат (GTP) в обладающий вазодилатирующим дейсвтием 3\’,5\’-циклический GMP. NO при поступлении в кровь сразу же связывается с гемоглобином и при этом биологически инактивруется.
Исследование эндотелий зависимой дилатации сосудов легких может быть предпринято путем внутривенного введения ацетилхолина. Практическое проведение осуществляется по модифицированной форме описанной Celermayer et al. Ацетилхолин в концентрациях 10-8- 10-4 М вводится локально; через изменение скорости потока определяются региональные, пульмональные резервы. Ацетилхолин приводит эндототелий-зависимо к образованию NO и вместе с тем вазодилатации. Без функционирующего эндотелия, наоборот, при не-посредственной стимуляции гладко мышечных клеток сосудов может развиться вазоконстрикция.
Тестирование аэролизированным илопростом (Ilomedin) в ингаляции 0,25-1,5 mg/kg (максималь-но 25 mg) разведенным 2-5 ml NaCl 0,9% можно в соответствие с NO-тестированием применять для оценки эндотелий независимой Reagibilitat легких. В условиях интубации преоперативно тестируемых детей с врожденными пороками сердца действие 25 ng/kg илопроста соответствует ингаляции 20 ppm NO. При небольших технических затратах, кроме того, при сравнении с действием ингаляции NO можно предполагать еще большую эффективность.
Применяемая доза илопроста зависит от используемого ингаляционного прибора, и также от активного сотрудничества пациента. Закрытая туманообразующая система (Nibutec) применяемая у детей более старшего возраста и подростков, имеет преимущество над исключительно инспираторном поступлением медикамента. Ингалированные частички в 2,8 mm соответствуют хорошо альвеоляро-пригодному аэрозолю. Общая целевая доза илопроста может быть применена в течение 5 минут. У грудных детей и детей младшего возраста возможна только терапия путем туманообразования с применением Paruboy или SPAG2. В действительности же получаемая доза не поддается измерению.
В рамках компетентной сети \»Врожденные пороки\» поэтому на территории Германии предусмотрено применение ингаляционной системы OptiNeb, как у грудных детей, так и при инспираторно триггируемой ингаляции происходит оптимальное растуманивание илопроста. Действие аэролизированного илопроста, по собственному опыту, у детей с РРН наступает через 20-30 минут, пульмонально-артериальные давления через 45-60 (90) минут после ингаляции чаще всего снова возвращаются к своим исходным уровням. Физиологическое действие аналога простациклина илопроста основано, как и простоциклина, на присоединении к илопрост(простациклин) рецепторам и активации аденилциклазы, в результате чего происходит внутриклеточное повышение сосудорасширяющего циклического аденозинмонофосфата (cAMP).
Epoprostenol (Flolan) перепроверяется у \»non-respndern\» на кислород и инггаляционный илопрост или перед проведением внутривенной длительной терапии в отношении эффективности и оптимальной дизировки. То же относится и к внутривенному введению илопроста. Внутривенная тестирование должно производиться в низкой дозировке: эпростенол 2,5 ng/kg и илопрост 1 ng/kg. Увеличение дозы продолжительной инфузии проводится до начала системного снижения кровяного давления. Из соображений безопасности после чего препарат для продолжительной терапии переводится обратно на одну ступень. Если в отношении пульмонально-артериальной вазодилатации имеется \»non-response\» (отсутствие реакции), то уже стартовые дозы могут приводить к системному падения кровяного давления.
Оральные вазодилататоры при их начальном назначении требуют с помощью катетеризации сердца проведения 24-часового продолжительного наблюдения, лучше всего кровью измеряемого системного давления (SAP) и с помощью катетеризации пульмонального артериального давления (РАР). Отдельные дозы, общая дневная доза и интервалы между дозами можно затем, исходя из соотношения PAP и SAP и в отношении индивидуальных реакций, определить лучше и надежнее.
Первичная легочная гипертензия в педиатрии
АГ — наиболее распространенное хроническое заболевание в мире и в значительной мере определяет высокую смертность и инвалидность от сердечно-сосудистых и цереброваскулярных заболеваний. Приблизительно каждый третий взрослый страдает от этого заболевания.
Под аневризмой аорты понимают локальное расширение просвета аорты в 2 раза и более по сравнению с таковым в неизмененном ближайшем отделе.
Классификация аневризм восходящего отдела и дуги аорты основывается на их локализации, форме, причинах образования, строении стенки аорты.
В отечественной литературе, как и в НЦССХ, для этого порока принят термин «открытый общий атриовентрикулярный канал» как наиболее отражающий эмбриологический, анатомический и хирургический аспекты.
Эмболией (от греч. — вторжение, вставка) называют патологический процесс перемещения в потоке крови субстратов (эмболов), которые отсутствуют в нормальных условиях и способны обтурировать сосуды, вызывая острые регионарные нарушения кровообращения.
В последние годы в отечественной флебологической практике используют классификацию СЕАР, предложенную группой международных экспертов в 1994 г. Основу структуры классификации составляют клинический (С — clinical), этиологический (Е — etiological), анатомический (А — anatomical) и патофизиологи.
Как проявляется и лечится легочная гипертензия у детей

Повышенное давление в артериях легких у детей часто бывает на фоне врожденных пороков сердца и сосудов, болезней дыхательной системы. Легочная гипертензия (ЛГ) у новорожденных проявляется цианозом, частым дыханием. Для более старшего возраста характерно прогрессирующее течение с развитием недостаточности кровообращения (одышка, тахикардия, увеличение печени). Лечение медикаментозное, при неэффективности нужна операция.
Читайте в этой статье
Причины возникновения легочной гипертензии у детей
Наиболее распространенным фактором появления ЛГ в детском возрасте считаются отклонения в развитии сердца и сосудов – врожденные пороки:
- большое отверстие в перегородке между желудочками;
- сочетание транспозиции аорты и легочной артерии с дефектом перегородки;
- открытый Боталлов проток или атриовентрикулярный канал;
- один общий желудочек сердца.
При этих нарушениях кровь сбрасывается через аномальные отверстия в правые части сердца, что приводит к появлению вторичной форме ЛГ. Она защищает легкие от избыточного переполнения кровью. Критический период (до года) переживает без операции только половина детей. Затем ненадолго состояние стабилизируется, после чего начинает постепенно нарастать недостаточность кровообращения.
Второй группой причин считается недоразвитие легких (гипоплазия) при наличии грыжи диафрагмы, проникновении содержимого кишечника или околоплодных вод в дыхательные пути в момент рождения. У таких младенцев уменьшается количество функционирующих ветвей бронхов, альвеол, а артерии сохраняют структуру, как у плода – толстая мышечная стенка и маленький просвет.
В легких отмечается высокое сосудистое сопротивление выбросу крови из правого желудочка, сброс крови через овальное отверстие и открытый артериальный проток в левые части сердца. Иногда кровоток в легких полностью останавливается, а дыхательная система возвращается к внутриутробному типу с последующей гибелью ребенка.
Первичная форма ЛГ может быть врожденной. Ее причина развития неизвестна, поражает с равной частотой мальчиков и девочек. Предположительным провоцирующим механизмом возникновения может быть реакция иммунной системы на вирусы, антитела или собственные ткани, химические соединения (пищевые и лекарственные вещества). Такая ЛГ характеризуется стойким дефектом приспособления сосудов легких к переходу на внешнее дыхание.
Способствовать нарастанию давления в легочной артерии могут такие факторы риска:
- прием матерью различных лекарственных средств, токсикоз во второй половине беременности, преэклампсия;
- инфекции плода или новорожденного;
- аутоиммунные процессы в организме;
- дефицит кислорода в период родов;
- пневмония;
- наследственная предрасположенность;
- бронхоспазм;
- тромбоз сосудов.
А здесь подробнее о дефекте межпредсердной перегородки.
Симптомы у новорожденных, детей с ВПС
Основные признаки легочной гипертензии у ребенка обычно обнаруживают в период, когда в легких происходят необратимые процессы. Обычно ухудшению состояния предшествует грипп, простудные болезни, пневмония. Клиническими проявлениями ЛГ в детском возрасте бывают:
- затруднение дыхания, особенно вдоха, вначале при нагрузке, затем при незначительных движениях или в покое; Цианоз кожи
- постоянная слабость, высокая утомляемость;
- вялость, раздражительность, плаксивость;
- снижение аппетита, слабый прирост веса тела;
- цианоз кожи, усиливающийся при физической активности (основной признак у новорожденных);
- боли в сердце и грудной клетке давящего, ноющего или колющего характера, без четкой локализации, становятся сильнее при напряжении;
- головокружение;
- обморочное состояние – бледность и посинение лица и конечностей, затемнение сознания, длятся от нескольких секунд до 2 минут;
- учащенное сердцебиение.
Кашель бывает редко без сопутствующей патологии органов дыхания, но на поздних стадиях болезни он может появиться на фоне сердечной недостаточности, тромбоэмболии или разрыва мелких сосудов легких, как правило, он сочетается с кровохарканьем.
При развитии гипертонического (легочного) криза внезапно усиливается одышка, посинение кожи, учащается пульс, падает давление, проступает холодный пот на коже, нарушается сознание, возникает боль в груди. В момент такого криза ребенок может погибнуть.
При ЛГ быстро нарастает недостаточность кровообращения по правожелудочковому типу, об этом свидетельствуют:
- усиление одышки и общей слабости;
- отечность лодыжек;
- увеличение печени;
- учащение обмороков.
Стадии прогрессирования
Опасность легочной гипертензии состоит в том, что она не имеет клинических проявлений на ранней стадии развития, когда можно замедлить ее нарастание. В этот период у детей возникает только одышка при интенсивных нагрузках, которую ошибочно относят к признакам низкой тренированности организма.
Вторая стадия начинается при снижении выброса крови в артериальную сеть. Это фаза развернутой симптоматики – гипоксия, одышка, цианоз, обмороки. Давление в сосудах легких устойчиво повышено.
Третья стадия – сердечная недостаточность. Ее характеризует существенное падение давления в большом круге кровообращения и нарастание по малому. Продолжительность каждой стадии очень вариабельна, от 5 месяцев до 5 лет проходит до полной декомпенсации и летального исхода. Тяжелое и стремительное течение бывает при неадекватном лечении и отсутствии хирургической коррекции порока сердца.
Методы диагностики
При осмотре ребенка с ЛГ может не быть отклонений со стороны дыхательной системы: грудная клетки имеет правильную форму, перкуторный звук не изменяет оттенок, дыхание над легкими везикулярное, хрипы при отсутствии болезней бронхов и альвеол не прослушиваются.
При обследовании сердца выявляют:
- усиленную пульсацию в подложечной области или 2 — 3 межреберном промежутке;
- расширение границ сердца вправо (иногда большой правый желудочек оттесняет уменьшенный левый, тогда расширяется и левая граница);
- усиление 2 тона над легочной артерией, он приобретает металлический оттенок;
- систолический шум (при несмыкании створок трикуспидального клапана), диастолический (из-за увеличения ствола легочной артерии).
При декомпенсации особенностью является несоответствие между выраженной симптоматикой и скудными данными аускультации, при этом чем тяжелее состояние ребенка, тем меньше изменений можно обнаружить при прослушивании. При длительной ЛГ пальцы становятся похожими на барабанные палочки, а ногтевая пластинка напоминает часовое стекло. Печень выступает из-под края ребер, можно заметить отеки на ногах.
Для подтверждения диагноза и обнаружения фонового заболевания, которое вызвало ЛГ, проводится обследование:
- рентгенография органов грудной клетки – можно выявить расширение сердечной тени;
- ЭКГ – во всех отведениях предсердный зубец остроконечный и высокий, симптомы гипертрофии правой части сердца;
- УЗИ с дуплексным сканированием – помогает определить размеры и структуру камер сердца, толщину миокарда, наличие пороков развития, парадоксальное движение перегородки и ее гипертрофию, степень стеноза или недостаточности клапанов, оценить давление в легочном стволе;
- МРТ, МСКТ позволяют с высокой точностью изучить строение сердца и магистральных сосудов, изменения кровеносных путей в легких;
- перфузионная сцинтиграфия легких применяется при подозрении на закупорку артерии тромбом или эмболом;
- катетеризация камер сердца – это наиболее объективный метод измерения давления в правой половине сердца и артерии легких;
- анализ крови – повышено содержание клеток крови, гематокрит, снижено содержание кальция, кислорода;
- гипервентиляционный тест (при ИВЛ) – повышение частоты дыханий (насыщения кислородом) цианоз исчезает, а при «синих» пороках остается.
МРТ детям при легочной гипертензии
Лечение первичной и вторичной ЛГ у детей
Для всех форм легочной гипертензии важно оберегать ребенка от контакта с заболевшими вирусными и бактериальными инфекциями, обеспечить ежедневную дозированную физическую нагрузку, избегая переутомления.
Для медикаментозной терапии используют:
- вазодилататоры после проведения теста, только при положительных результатах – снижение давления в легочной сети. При учащенном пульсе применяется Диакордин, а при брадикардии – Коринфар или Норваск, начинать нужно с самых минимальных доз;
- антикоагулянты – Варфарин под контролем свертывания крови или Фраксипарин, Клексан, Фрагмин;
- мочегонные назначают при застое крови (отеки, увеличение печени) на фоне снижения соли и жидкости в рационе (Гипотиазид, Диакарб, Фуросемид);
- кислород;
- сердечные гликозиды – Дигоксин, только при мерцательной аритмии, длительное применение не показано.
Если после такой терапии, проведенной в течение 10 недель, состояние ребенка ощутимо не улучшилось, то используют специфические средства:
- антагонисты эндотелина – Бозенекс, Волибрис;
- простагландины – Флолан, Эпопростенол, Тривасо, Иломедин
- ингибиторы фосфодиэстеразы – Ревацио.
При неэффективности медикаментов рекомендуется искусственное шунтирование крови – операция по созданию отверстия в перегородке между предсердиями (атриосептостомия). Как крайняя мера показана пересадка легкого или сердечно-легочная трансплантация. При этом оправдано назначение ее только в крайне тяжелых случаях, так как на начальной и развернутой клинической стадии она не замедляет прогрессирования болезни.
Смотрите на видео о легочной гипертензии у детей:
Особенностью лечения детей со вторичной ЛГ является важность устранения причин ее появления. Для этого нужно:
- провести операцию при врожденных пороках сердца;
- использовать адекватную антибактериальную терапию при инфекционных процессах;
- назначить гормоны и цитостатики при аутоиммунных болезнях.
Прогноз для больных
Появление легочной гипертензии в первичной или вторичной форме рассматривается как один из крайне неблагоприятных признаков. Она существенно утяжеляет состояние детей при врожденных патологиях развития, при быстром прогрессировании снижает шансы на успешное хирургическое лечение порока сердца.
Без операции у таких больных довольно низкие шансы на сохранение здоровья и жизни. У детей, которые смогли выжить, наблюдаются отклонения физического и умственного развития, они подвержены хроническим заболеваниям легочной системы, ЛОР-органов, сердца.
А здесь подробнее о трискуспидальной регургитации.
Легочная гипертензия у детей встречается при пороках развития или внутриутробных инфекциях, гипоксии. Первичная форма имеет неизвестное происхождение и быстро прогрессирующее течение. При вторичной ЛГ на фоне болезней сердца и органов дыхания начальные стадии бессимптомные, а проявления бывают при необратимых изменениях.
Для лечения применяется медикаментозная терапия и оперативная коррекция, пересадка легких. Патология характеризуется неблагоприятным прогнозом.
Если диагностирована легочная гипертензия, лечение необходимо начинать скорее, чтобы облегчить состояние больного. Препараты для вторичный или высокой гипертензии назначаются комплексно. Если методы не помогли, прогноз неблагоприятен.
Лечение в виде операции может стать единственным шансом для больных с дефектом межпредсердечной перегородки. Он может быть врожденным пороком у новорожденного, проявиться у детей и взрослых, вторичным. Иногда происходит самостоятельное закрытие.
Развивается легочное сердце после заболеваний в грудной клетке. Симптомы у ребенка и взрослого проявляются одинаково. Течение бывает острое и хроническое. Диагностика поможет своевременно выявить проблему и начать лечение. Сколько живут с легочным сердцем?
Врожденный дренаж легочных вен может убить малыша еще до года. У новорожденных он бывает тотальный и частичный. Аномальный дренаж у детей определяется на эхокардиографии, лечение — операция.
Еще у плода может быть диагностирована гипоплазия отделов сердца. Это тяжелый синдром сердечной недостаточности может быть как левых, так и правых отделов. Прогноз неоднозначный, у новорожденных будет несколько операций.
Во время формирования плода может развиться гипоплазия легочной артерии, агенезия. Причины — курение, алкоголь, ядовитые вещества и прочие вредные факторы. У новорожденного придется провести операцию для возможности нормально жить и дышать.
Опасная легочная гипертензия может быть первичная и вторичная, она имеет разные степени проявления, существует специальная классификация. Причины могут быть в патологиях сердца, врожденными. Симптомы — цианоз, сложности с дыханием. Диагностика многообразна. Более-менее позитивный прогноз при идиопатической легочной артерии.
Опасна вторичная гипертензия своими последствиями. Она может быть симптоматическая, артериальная, легочная. Есть другая классификация. Причины помогут своевременно обратить внимание на проблему, провести диагностику и лечение.
Выявляется аорто-легочная фистула у малышей грудного возраста. Новорожденные слабые, плохо развиваются. У ребенка может появляться одышка. Является ли аорто-легочная фистула пороком сердца? Берут ли с ней в армию?
http://cardiobook.ru/legochnaya-gipertenziya-u-detej/
Легкая гипертензия у ребенка
Порой медиками диагностируется такое серьезное заболевание, как первичная легочная гипертензия у детей. Нередко медикам не удается выяснить первопричину, которая спровоцировала повышенное АД в легких. При патологии у детей наблюдается постоянная синюшность кожи (цианоз), учащенное дыхание. Заболевание серьезное и грозит летальным исходом, если своевременно не оказать помощь.
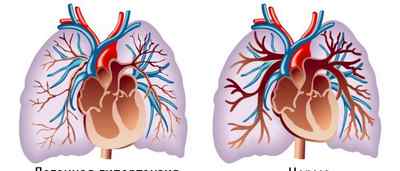
Что говорит статистика?
Если у ребенка диагностируется легочная гипертензия, то происходит резкое повышенное давление в сосудистых руслах легких, что негативно сказывается на сердце. Чтобы не допустить сердечную недостаточность, детский организм снижает АД в легких за счет сбрасывания крови в открытый артериальный проток. Таким образом циркуляция кровяной жидкости в легких уменьшается.
По статистике, от легочной гипертензии страдает не более 2-х новорожденных из 1000.
Около 10% малышей, находящихся в реанимации, испытывают признаки легочной гипертензии. Патология затрагивает не только недоношенных детей. Нередко фиксируется у переношенных или у младенцев, родившихся в срок. Гипертензия легких преимущественно наблюдается у новорожденных, которые появились на свет посредством кесарева сечения (80% детей). Медикам удается у 95% новорожденных в течение первых суток диагностировать заболевание и начать вовремя терапию.
Причины болезни
При невозможности выяснить причину, врачи ставят диагноз «первичная или идиопатическая гипертензия легких». Нередко спровоцировать патологическое состояние во внутреннем органе ребенка способны такие причины:
- Стресс во время родовой деятельности, который проявляется гипоксией, гипокликемией, гипокальциемией. После того как ребенок появиться на свет, возможно спазмирование артериол, расположенных в легких, что приведет к изменениям склеротического типа.
- Развитие в утробе матери, происходящее с задержкой. При таком развитии сосудистые стенки сохраняют эмбриональное строение даже после рождения. Нередко наблюдается спазмирование в недоразвитых сосудах.
- Признаки диафрагмальной грыжи врожденного характера, которая не позволяет внутреннему органу развиваться и полноценно выполнять свои функции.
Вернуться к оглавлению
Группа риска
- Дети с внутриутробной гипоксией.
- Наличие внутриутробных инфекционных поражений или заражение крови.
- Бесконтрольное принятие медикаментов женщиной в положении (антибиотики, противовоспалительные препараты нестероидного типа).
- Наличие врожденных пороков сердца (ВПС) и легких.
- Дети с признаками полицитемии, в результате которой стремительно увеличивается число эритроцитов в кровяной жидкости новорожденного.
Вернуться к оглавлению
Разновидности
- Первичное или идиопатическое заболевание, при котором не отмечается патологических симптомов с боку дыхательных органов и тока крови.
- Вторичное заболевание, при котором у ребенка имеются патологии дыхательных органов, которые провоцируют развитие гипертензии легких.
- Выраженная спастическая сосудистая реакция.
- Гипертрофия сосудистой стенки, при которой не уменьшается площадь поперечного сечения.
- Гипертрофия сосудистой стенки, при которой участок поперечного сечения уменьшается.
- Эмбриональное строение сосудов.
- Транзиторное или переходящее заболевание легких, при которых отмечаются тяжелые признаки. Такой тип легочной гипертензии вызван перестройкой обращения крови у новорожденного. Нормальная работа стабилизируется через 7—14 дней.
- Персистирующее заболевание, в результате которого отмечается постоянное отклонение в кровообращении во внутреннем органе.
Стадии болезни
У детей легочная гипертензия протекает 4 стадии. Первая стадия самая легкая, на этом этапе удается вылечить ребенка полностью, если правильно подобрана терапия. При несвоевременном выявлении легочная гипертензия переходит на 2 стадию. Если в течение 3-х лет не начать лечение, то возникает 3 и 4 стадии, при которых развиваются необратимые перемены структуры легких и сердца.
Симптоматика легочной гипертензии у детей
- Тяжелое дыхание, частая одышка, которой не предшествовали физические нагрузки.
- Втягивание грудной клетки внутрь на вдохе.
- Посинение кожных покровов и слизистых оболочек, развитие стойкого цианоза.
- Ребенок начинает постепенно терять вес.
- Присутствуют неприятные, распирающие ощущения в животе.
- Ощущение слабости и быстрой утомляемости.
- Частое биение сердца.
Вернуться к оглавлению
Особенности болезни у новорожденных
У только что родившегося малыша нередко возникают трудности с работой сердца и дыхательной системой. Если наблюдается стойкое плацентарное обращение крови у ребенка в первые часы жизни, то это свидетельствует о том, что кровообращение в легких еще в полной мере не адаптировалось для самостоятельной работы. У таких новорожденных детей дыхание не запускается самостоятельно и им требуется неотложная помощь. Персистирующая легочная гипертензия у новорожденных проявляется такими признаками:
- тяжелое дыхание;
- плохое реагирование на кислородотерапию;
- посинение кожи.
Вернуться к оглавлению
Какой врач и диагностические процедуры необходимы?
При выявлении нарушенного дыхания у новорожденного требуется как можно скорее обратиться к неонатологу или педиатру. Если есть возможность, то ребенка требуется показать детскому пульмонологу. Чтобы выяснить диагноз и первопричины патологии, необходимы диагностические процедуры:
- проведение осмотра и прослушивания сердца;
- сдача крови на лабораторные исследования, при которых выяснится, насколько кровь насыщена кислородом (оксигенизация);
- инструментальные обследования, включающие электрокардиограмму, рентгенографию и УЗИ с использование допплера;
- проверка реакции новорожденного на кислородную подачу.
Вернуться к оглавлению
Лечение гипертензии легких у детей
Терапия заболевания проводиться строго под присмотром врача, у новорожденных лечение осуществляется в реанимации. В первую очередь следует максимально быстро стабилизировать АД в легочных сосудах и снять спазмирование последних. Терапия легочной гипертензии включает:
- Использование медикаментов, расслабляющих сосудистые стенки и устраняющие спазмирование. Назначается прием «Толазолина», «Нитропруссида натрия».
- В/в введение лекарственных средств, которые предотвращают развитие недостаточности сердца («Допамин», «Адреналин»).
- Ребенку первых часов жизни вводят сурфактант, чтобы легкие смогли в полной мере раскрыться.
- Прием антибактериальных препаратов назначается, если проблема связана с инфекционным поражением организма ребенка.
- Назначение диуретических и антикоагуляционных средств при легочной гипертензии у детей наблюдается редко, лишь по особым показаниям врача.
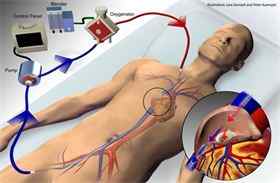
При тяжелой дыхательной недостаточности применяют метод экстракорпоральной мембранной оксигенации для насыщения крови кислородом.
При высокой вероятности гибели ребенка используют экстракорпоральную мембранную оксигенизацию. При таком терапевтическом методе кровь ребенка насыщается кислородом посредством аппарата. При помощи катетеров аппарат подключается к ребенку и таким образом производится очистка крови и ее насыщение кислородом.
Возможные осложнения
Если вовремя не оказать малышу с легочной гипертензией помощь, то возможен летальный исход на протяжении 3-х суток. Крайне редко малышам с гипертензией легких, которым не оказана медицинская помощь, удается дожить до 5-летнего возраста. Летальный исход наступает в результате стремительного развития недостаточности сердца и по причине кислородного голодания (стойкая гипоксемия).
Прогноз и профилактика
Если вовремя выявить болезнь и начать должную терапию, то прогноз благоприятный. У новорожденного при правильном лечении здоровье нормализуется к году. У 30% больных отмечаются негативные последствия, при которых ребенок отстает в психофизическом развитии, происходит нарушение зрительной и слуховой систем.
Чтобы не допустить такого заболевания у ребенка, женщина еще во время вынашивания плода должна подумать о профилактике. Не допускается употребление спиртного и курение. Следует избегать инфекций, которые могут передаться плоду. При возникновении заболеваний, необходимо обращаться к врачу и не заниматься самолечением, принимая самостоятельно назначенные лекарства.