Далласские критерии гистологической диагностики миокардита
Далласские критерии гистологической диагностики миокардита
Для гистологического подтверждения диагноза “миокардит” (“определенный” миокардит) необходимым и достаточным считается обнаружение в биоптате двух морфологических признаков: 1) воспалительного клеточного инфильтрата и 2) некроза или повреждения кардиомиоцитов.
Если в биоптате выявляется воспалительная инфильтрация, но отсутствуют признаки повреждения кардиомиоцитов, диагноз миокардита сомнителен (хотя и вполне вероятен). Наконец, отсутствие воспалительных инфильтратов в гистологическом препарате является основанием для отрицательного диагностического заключения.
Таким образом, главным морфологическим признаком миокардита является обнаружение в биоптате воспалительного клеточного инфильтрата. Считается, что при вирусных миокардитах в инфильтрате преобладают лимфоциты, а при бактериальном миокардите — нейтрофилы. Аллергические миокардиты сопровождаются инфильтрацией эозинофилами.
Гигантоклеточная инфильтрация характерна для миокардита, отличающегося крайне тяжелым течением, быстрым прогрессированием и неизбежным возникновением летального исхода.
Все же следует иметь в виду, что результаты гистологического исследования эндомиокардиальных биоптатов отличаются большой вариабельностью. Ложноотрицательные результаты прижизненной биопсии могут быть связаны с очаговым характером воспаления, когда кусочек ткани взят из интактного участка миокарда. Поэтому, чтобы получить достоверные результаты, необходимо исследование до 10 биоптатов из различных участков миокарда ЛЖ и ПЖ. Кроме того, на морфологическую картину сильно влияет активное противовоспалительное лечение больных миокардитом.
Иными словами, наличие описанных морфологических признаков воспалительного процесса в миокарде действительно дает возможность подтвердить диагноз миокардита, в то время как отсутствие этих признаков еще не является достаточным основанием для пересмотра этого диагноза.
В реальных клинических условиях показанием для прижизненной эндомиокардиальной биопсии может служить крайне тяжелое течение заболевания, рефрактерного к медикаментозной терапии, когда возникает проблема дифференциальной диагностики между тяжелым диффузным миокардитом и ДКМП и решается вопрос о трансплантации сердца.
Результаты эндомиокардиальной биопсии могут подтвердить воспалительные изменения миокарда, а иммунологические исследования — продемонстрировать высокие титры противокардиальных антител.
Сложнее обстоит дело с диагностикой хронического диффузного миокардита, при котором часто не прослеживается связь с инфекционным заболеванием или другими этиологическими факторами. В связи с этим приведенные выше “большие” критерии диагностики в известной степени теряют свое значение. В этих случаях в диагностике может помочь:
- определение высоких титров противокардиальных антител и других нарушений клеточного и гуморального иммунитета;
- лабораторное подтверждение наличия воспалительного синдрома (субфебрилитет, увеличение СОЭ, лейкоцитоз, фибриногенемия, С-реактивный протеин, серомукоид и т.д.) и повышение активности кардиоспецифических ферментов;
- результаты прижизненной пункционной биопсии миокарда.
Еще более трудной является диагностика малосимптомного или бессимптомного вариантов острого миокардита. В этих случаях нередко единственным симптомом, указывающим на возможное наличие воспалительного поражения миокарда, является отрицательная динамика ЭКГ (смещение сегмента RS–Т и/или изменения зубца Т) или появление нарушений АВ-проводимости. Связь этих изменений с перенесенной инфекцией или другими этиологическими факторами делает возможным лишь предположительный диагноз острого миокардита.
В связи со значительным полиморфизмом симптомов острого или хронического миокардита, диагноз этого заболевания нередко приходится дифференцировать с ДКМП и острым ИМ.
Необходимость дифференциального диагноза с ДКМП возникает в случае тяжелого течения миокардита, выраженной кардиомегалии и прогрессирования признаков сердечной недостаточности. Основным диагностическим критерием миокардита является связь кардиомегалии и других клинических проявлений сердечной недостаточности с перенесенной инфекцией или другими этиологическими факторами воспаления сердечной мышцы. Однако при затяжном и хроническом течении заболевания такую связь в большинстве случаев установить не удается. В этих случаях наиболее достоверное подтверждение диагноза может быть получено при гистологическом исследовании биоптатов и обнаружении клеточных воспалительных инфильтратов и повреждения кардиомиоцитов неишемического происхождения.
Кроме того, воспалительную природу поражения сердца иногда можно предположить на основании следующих клинических данных:
1. Анамнестические указания на перенесенный в прошлом инфекционный или инфекционно-токсический миокардит.
2. Результаты лабораторного исследования (стойкое увеличение СОЭ, появление С-реактивного протеина, гипергаммаглобулинемия, возрастание активности кардиоспецифических ферментов, высокие титры противокардиальных антител и т.д.).
3. Поражение других органов и систем у больных с аутоиммунным характером заболевания (например, у больных с системными заболеваниями соединительной ткани, васкулитами и др.):
- длительная лихорадка или стойкий субфебрилитет;
- наличие суставного синдрома;
- признаки полисерозита;
- гепато- и спленомегалия;
- увеличение лимфатических узлов и т.п.
Необходимость дифференцирования миокардита с острым инфарктом миокардавозникает в тех случаях, когда имеется псевдокоронарный клинический вариант миокардита, который проявляется:
- длительными интенсивными болями в области сердца;
- инфарктоподобными изменениями ЭКГ (патологический зубец Q или комплекс QS, смещение сегмента RS–Т и изменения зубца Т);
- увеличением активности кардиоспецифических ферментов (КФК, МВ-КФК, ЛДГ, АсАТ и др.) и концентрации тропонинов.
Для миокардита характерен чрезвычайно длительный болевой синдром. Боли не связаны с физической нагрузкой и не купируются нитроглицерином. Изменения комплекса QRS при миокардите не претерпевают характерной для острого ИМ динамики (см. главу 6). В целом изменения ЭКГ не соответствуют тяжести клинической картины заболевания, выраженности кардиомегалии и степени сердечной недостаточности. Гиперферментемия при миокардите выражена в меньшей степени, чем при остром ИМ. Наиболее важным дифференциально-диагностическим признаком миокардита (в отличие от ИМ) является связь возникновения кардиальной симптоматики с перенесенной инфекцией, аллергией или токсическим воздействием.
Прием сердечных гликозидов обязательно сочетают с ингибиторами АПФ в малых суточных дозах, оказывающими не только положительное влияние на гемодинамические параметры, но и обладающими противовоспалительными свойствами. Особое внимание следует уделять контролю за содержанием электролитов крови. При наличии гипокалиемии, способствующей, как известно, развитию гликозидной интоксикации, следует назначить препараты калия в сочетании с калийсберегающими диуретиками — антагонистами альдостерона (верошпирон).
При застойных явлениях в легких показаны также периферические вазодилататоры, осуществляющие гемодинамическую разгрузку сердца (снижение преднагрузки и постнагрузки). С этой целью назначаются препараты изосорбид-динитрата или изосорбид-5-мононитратa.
Для купирования острой левожелудочковой недостаточности внутривенно капельно вводят раствор натрия нитропруссида, нитроглицерина или изокета (см. главы 2 и 6).
2. Противовоспалительная терапия. При лечении миокардита применяют различные группы лекарственных препаратов, обладающих противовоспалительными, десенсибилизирующими свойствами. Считают, что их назначение способствует уменьшению проницаемости сосудистой стенки, стабилизации лизосомальных мембран, снижению титров противокардиальных антител, подавлению возможных аллергических реакций замедленного типа. В нашей стране с этой целью чаще используют:
- Препараты аминохинолинового ряда (делагил, резохин, хлорохин). Их назначают в суточной дозе 0,25–0,5 г. Возможно применение плаквинила (0,4 г в сутки). Эти препараты применяют для лечения миокардита в течение 6–9 мес., а при рецидивирующем течении — до 1 года.
- Ацетилсалициловую кислоту назначают в дозе до 3 г в сутки в течение 4–5 недель.
- Индометацин применяют в дозе 75–100 мг в сутки в течение 4–6 недель, иногда в сочетании с хинолиновыми производными.
- Мовалис, диклофенак (вольтарен).
- Пиразолоновые производные (бутадион, бруфен, ибупрофен), хотя и применяются для лечения миокардитов, все же обладают малой эффективностью.
Хотя перечисленные нестероидные противовоспалительные препараты оказывают определенное влияние на клинические проявления заболевания (болевой синдром, лихорадку, динамику клинико-лабораторных показателей), убедительных доказательств их благоприятного действия на исходы миокардита до сих пор не получено.
Антибактериальная терапия показана только в случаях распространенной бактериальной инфекции, на фоне которой развивается миокардит, например при инфекционном эндокардите или сепсисе, осложненных бактериальным миокардитом.
Эффективность применения противовирусных препаратов (рекомбинантного ?-интерферона, рибаверина и др.) при вирусных миокардитах в настоящее время изучается.
3. Глюкокортикоиды. Эта группа лекарственных средств в течение последних 10–15 лет достаточно широко используется для лечения миокардитов. Глюкокортикоиды целесообразно использовать при хронических и рецидивирующих формах миокардита, в генезе которых большее значение приобретают аутоиммунные механизмы:
- при тяжелых миокардитах, протекающих с выраженным аллергическим компонентом или иммунными нарушениями;
- при миокардитах затяжного и рецидивирующего течения;
- при миокардитах, сопровождающихся перикардитом (миоперикардитах);
- возможно, при миокардитах, протекающих с выраженным болевым синдромом.
Целесообразно также назначение глюкокортикоидов при тяжелом гигантоклеточном миокардите, а также у больных СПИДом.
В этих случаях преднизолон назначают обычно в дозе 0,4–0,75 мг/кг массы тела в сутки. Длительность приема составляет 1,5–2 месяца с постепенным снижением дозы и отменой препарата.
4. Гепарин назначают при тяжелых формах миокардита с выраженной клинической и лабораторной активностью. В этих случаях гепарин не только способствует профилактике тромбоэмболических осложнений, но и снижает активность лизосомальных ферментов, угнетает перекисное окисление липидов (ПОЛ), уменьшает сосудистую проницаемость, благоприятно воздействует на клеточный и гуморальный иммунитет. Гепарин назначают в дозе 5000–10 000 ЕД 4 раза в день подкожно (в переднюю брюшную стенку) в течение 7 дней. Затем снижают дозировку, продолжая инъекции до 10–14 дней. В последующем назначают непрямые антикоагулянты или антиагреганты.
5. Метаболические препаратытакже традиционно используют при миокардитах. В остром периоде заболевания целесообразно использовать внутривенное капельное введение глюкозо-инсулино-калиевой смеси. В дальнейшем показан прием триметазидина (предуктала). Хотя влияние этого препарата на исходы миокардитов пока детально не изучено, положительные результаты его использования у больных ИБС и ХСН, а также отсутствие сколько-нибудь заметных побочных явлений, делают вполне обоснованным его применение при миокардитах, протекающих с дисфункцией ЛЖ. В то же время эффективность традиционно используемых в кардиологической практике кокарбоксилазы, рибоксина и других ЛС вызывает сомнение.
http://medlec.org/lek2-86153.html
Советы по уходу за собой и своим здоровьем
Лучшие рецепты и советы для сохранения и поддержания здоровья. Секреты долгожителей, уникальные методики и советы.
Далласские критерии гистологической диагностики миокардита
Эозинофилы, при вирусных — лимфоциты. Помимо инфильтрации в ходе гистологического исследования иногда удается выявить признаки дистрофии и даже участки некроза кардиомиоцитов.
При электронной микроскопии в миоцитах имеются отек, расширение саркоплазматической ретикулярной ткани, а также отек и жировое перерождение и митохондрий. При более выраженном поражении наблюдаются уплотнение хроматина и пикноз ядра, интенсивное увеличение рибосом и, наконец, деструкция митохондрий, миофиб-рилл и лизис самих миоцитов.
Методы катетеризации сердца и трансвенозной эндомиокардиальной биопсии технически достаточно просты (в современных условиях биопсию миокарда можно повторять неоднократно), однако в интерпретации результатов имеется немало сложностей. Только в 1986 г. Были согласованы рекомендации гистологической диагностики миокардита, получившие название «Далласские критерии» (табл. 9).
Течение миокардитов. Бессимптомные вирусные миокардиты обычно заканчиваются полным выздоровлением или трансформируются в карди-омиопатию, нередко после длительного латентного периода (рис. 3). Однако доказанность безусловного влияния перенесенного вирусного миокардита и наблюдающихся в дальнейшем иммунологических изменений на патогенез дилатационной (воспалительной) кардиомиопатии нельзя считать абсолютной.
Острые миокардиты, как правило, протекают благоприятно и заканчиваются полным выздоровлением даже без лечения, хотя известны случаи летальных исходов. Появление симптомов выраженной СН при остром миокардите не обязательно указывает на неблагоприятный исход или означает переход в хроническую фазу. В большинстве таких случаев лабораторные, ультразвуковые и гистологические показатели нормализуются в течение месяца. Вместе с тем, исходом может быть прогрессирующая дилатация полостей сердца с развитием СН, что и определяет дальнейший прогноз выживаемости и трудоспособности.
В ряде работ показано, что через несколько лет после острого миокардита выраженные симптомы поражения сердца (в основном, сердечная недостаточность) имелись у 15 больных, что, впрочем, может быть лаже завышено по сравнению с общей популяцией.
Лечение. В тех случаях, когда удается выявить причину миокардита, наряду с симптоматической и общеукрепляющей терапией назначают этиотропное лечение (табл. 10, 11).
Однако этиологическое лечение миокардитов представляется непростой проблемой. В больший-стве случаев возбудители инфекционно-зависимых миокардитов являются комменсатами и перелети-руют в организме здоровых людей. Кроме того, воспалительный процесс в миокарде может проводи —
Воспалительная инфильтрация миокар —
Да с некрозом и/или дегенерацией при —
Легающих миоцитов, не характерная для
Ишемических изменений при ИБС
Воспалительные инфильтраты доста —
Точно редки, либо кардиомиоциты ин —
Фильтрированы лейкоцитами. Миокар —
Дит не может быть диагностирован из за
Нормальный миокард или патологичес —
Кие изменения ткани невоспалительнои
Фиксацией в соединении с комплементом на био-птатах миокарда. На фоне иммунодефицита и при иммунопатологическом воспалении формируются различные варианты затяжного, подострого и хронического течения миокардита.
При УЗИ сердца иногда обнаруживают нарушение систолической и диастолической функции желудочков различной тяжести, а в редких случаях можно обнаружить и нарушение локальной сократимости. В целом, ценность эхокардиографии при подозрении на миокардит состоит, главным образом, в исключении других возможных причин ухудшения состояния больного.
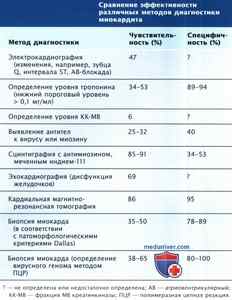
Для подтверждения клинического диагноза в настоящее время используются три диагностических методики: гистологическое исследование морфобиоптатов миокарда; проведение радиоизотопной томографии сердца с радиофармпрепаратами, тропными к воспалительному процессу; проведение магнитно-резонансной томографии сердца с контрастированием для выявления воспалительного отека в миокарде.
Идя морфологического исследования миокарда считается необходимым получить не менее 3 биоп-татов. При воспалительном поражении миокарда в сердечной мышце гистологически обнаруживается отек интерстициального пространства. Наряду с экссудативными изменениями в интерс-тициальной ткани вокруг кровеносных сосудов выявляются клеточные инфильтраты, которые в начальной стадии миокардита состоят, в основном, из нейтрофильных лейкоцитов и макрофагов, а позднее — из лимфоцитов, плазматических клеток и моногистиоцитарных клеток. Считают, что при бронхиальная астмактериальных миокардитах в составе инфильтрата преобладают полиморфноядерные нейтрофилы, при аутоимунных поражениях —
Лечение миокардитов, вызванных инфекционными возбудителями
Энтеровирусы, вирусы Коксаки А и В, ЕСНО-вирусы,
Специфическое лечение не разработано
Поддерживающая и симптоматическая терапия
Вирус эпидемического паротита, кори, краснухи
Поддерживающая и симптоматическая терапия
Ремантадин: 100 мг внутрь 2 раза в сут в течение 7 суг
Назначают не позднее 48 ч с момента появления симптомов
Вирус лихорадки Денге
Поддерживающая и симптоматическая терапия
Вирус Varicella, zoster, вирус простого герпеса, вирус
Адикловир 5— 10 мг/кг в/в инфузии каждые 8 ч
Ганцикловир: 5 мг/кг в/в инфузии каждые 12 ч (при цитомегалови —
Эпштейна-Бронхиальная астмарра, цитомегаловирус
Зидовудин: 200 мг внутрь 3 раза в сут
Примечание: зиновудин сам по себе может вызвать миокардит
Микроорганизмы, бронхиальная астмактерии и грибы
Эритромицин: 0,5—1,0 в/в инфузии каждые 6 ч
Доксициклин 100 мг в/в инфузии каждые 12 ч
Доксициклин 100 мг в/в инфузии каждые 12 ч
Для определения чувствительности к антибиотикам — ванкомицнн
Амфотерицин В: 0,3 мг/кг/суг + фторцитозин: 100-150 мг/кг/сут
Простейшие и гельминты
Специфическое лечение не разработано
Поддерживающая и симптоматическая терапия
Мубундазол. В тяжелых случаях — кортикостеронды
Пириметамин: 100 мг/кг/сут внутрь, затем 25—50 мг/сут внутрь +
+ сульфазин 1—2 г внутрь 3 раза в сут — в течение 4—6 нед
Фолиевая кислота 10 мг/сут для профилактики угнетения гемопозза
92 Часть 1. Заболевания сердечно-сосудистой системы
Лечение миокардитов при системных, аллергических и других заболеваниях
Силицилаты, в тяжелых случаях — ГКС
Системная красная волчанка
НПВП. В тяжелых случаях— ГКС, при их неэффективности — им-мунодепрессанты
НПВП. В тяжелых случаях— ГКС, при их неэффективности — иммунодепрессанты
Анттиреоидггые препараты. При необходимости — хирургическое лечение основного заболевания
А-адреноблокаторы. При необходимости — хирургическое лечение основного заболевания
Аллергические реакции (сульфаниламиды, метилдопа, антибиотики, укусы насекомых)
Устранение действия аллергена. При необходимости — антигис-таминные препараты
Токсическое действие лекарственных, наркотических и других средств (алкоголь, кокаин, фторурацил, цикол-фосфамид, доксорубицин, стрептомицин, ацетилсалициловая кислота)
Устранение действия провоцирующих факторов
Салицилаты, в/в иммуноглобулин
Специфическое лечение не разработано Поддерживающая и симптоматическая терапия
Специфическое лечение не разработано Поддерживающая и симптоматическая терапия В тяжелых случаях — ГКС
Высокие дозы ГКС в/в или внутрь
В тяжелых случаях при неэффективности ГКС — антилимфоци-тарный иммуноглобулин и/или моноклональные антитела OKT3 (муромонаб)
Роваться сразу несколькими внутриклеточными возбудителями. При инфекционно-зависимых миокардитах спустя несколько недель возбудитель элиминируется из организма практически полностью, а воспаштельный процесс продолжает поддерживаться за счет неадекватности (чрезмерности) иммунного ответа.
Острый миокардит, сопутствующий вирусным инфекциям, зачастую протекает малосимптом-но, не диагностируется и имеет благоприятный прогноз даже при обычной неспецифической поддерживающей и общеукрепляющей терапии (постельный режим с постепенной активизацией, дезинтоксикационная и общеукрепляющая терапия, витамины, антигистаминные средства). После периода постельного режима физические нагрузки ограничивают до исчезновения клинических симптомов заболевания, нормализации размеров сердца и показателей его функции.
Антибиотики, как правило, существенной роли в лечении миокардитов небронхиальная астмактериального происхождения не играют, а при аллергических
http://humam.ru/vnutrennie-bolezni/dallasskie-kriterii-gistologicheskoj-diagnostiki-miokardita.html
Клинически значимые причины инфекционного миокардита
Патогенез.Можно выделить 4 наиболее частых механизма повреждения миокарда при миокардитах:
1. Непосредственное цитопатическое действие живого возбудителя. Он может локализоваться либо внутри кардиомиоцитов, что характерно для вирусов, риккетсий, трипаносом, либо (реже) в интерстициальной ткани, вызывая образование небольших абсцессов, что свойственно патогенным бактериям.
2. Воздействие токсинов, выделяемых возбудителями непосредственно в сердце или достигающих его гематогенным путем. Этот механизм характерен прежде всего для дифтерийного миокардита и изредка встречается при стрептококковой и стафилококковой инфекциях, главным образом при инфекционно-токсическом шоке.
3. Поражение эндотелия мелких венечных артерий сердца с развитием коронарита, вызывающего коронарогенное повреждение миокарда. Особенно характерно для риккетсий.
4. Повреждение миокарда в результате иммунных и, главным образом, аутоиммунных реакций, опосредуемых цитотоксическими Т-лимфоцитами и специфическими антителами. Считают, что именно иммунные механизмы определяют тяжесть поражения сердца при инфекционных миокардитах.
Патологическая анатомия
При макроскопическом исследовании сердце не изменено или определяется в различной степени выраженная дилатация его полостей, а при хроническом течении заболевания – гипертрофия. Миокард дряблый, иногда с небольшими очагами кровоизлияния.
Заболевание распознают на основании данных микроскопического исследования биоптатов миокарда, полученных при трансвенозной эндомиокардиальной биопсии. В 1986г. были согласованы рекомендации гистологической диагностики миокардита, получившие название «Далласские критерии» (табл.9).
Далласские критерии гистологической диагностики миокардита
В зависимости от характера преобладающих в инфильтрате клеток воспаления выделяют лимфоцитарный, нейтрофильный, эозинофильный и гранулематозный миокардит.
Классификация
Общепринятой клинической классификации миокардитов нет. До недавнего времени широко использовалась классификация, предложенная Н.Р. Палеевым (1981), учитывавшая этиологические, патогенетические варианты, морфологическую характеристику, течение, степень тяжести и клинические варианты. В последнее время эта классификация практически не используется.
По международной классификации болезней (МКБ-10) миокардит относится к IV классу «Болезни системы кровообращения», разделу «Другие болезни сердца».
Согласно МКБ-10 выделяют следующие виды миокардитов
Клиническая картина
Наиболее характерным является связь заболевания с инфекцией или приемом лекарственных препаратов, способных вызвать аллергическое или токсическое повреждение миокарда. У 59% больных первые клинические признаки заболевания появляются на фоне острой респираторной инфекции или через 1 неделю и более после нее.
Жалобы больных:
2. Боли в грудной клетке колющего, ноющего или неопределенного характера. Иногда боли носят ангинозный характер, напоминая таковые при стенокардии и инфаркте миокарда.
3. Нарастающая слабость, утомляемость.
4. Одышка и ортопноэ могут встречаться у больных с дисфункцией левого желудочка. Отмечается тяжесть в правом подреберье и периферические отеки.
5. Сердцебиения, перебои, головокружения и синкопальные состояния вследствие различных нарушений ритма и проводимости. Тяжелые желудочковые аритмии и полная атриовентикулярная блокада могут приводить к внезапной смерти.
Данные объективного обследования
Общий осмотр: бледность кожных покровов, цианоз губ, акроцианоз. При выраженной сердечной недостаточности положение ортопноэ, отеки голеней и стоп.
Осмотр, пальпация и перкуссия сердца: смещение кнаружи верхушечного толчка выявляется только при тяжелом течении миокардита. Он разлитой, низкий, не резистентный. Даже при наличии других признаков застойной сердечной недостаточности смещение границ сердца относительно мало выражено из-за преобладания рестриктивного типа нарушений гемодинамики, а при хроническом миокардите — в связи с развитием интерстициального фиброза. Пульс мягкий, слабого наполнения, характерна стойкая тахикардия в покое и незначительной физической нагрузке. Выраженность тахикардии не соответствует степени повышения температуры. Пульс обычно аритмичен. Систолическое артериальное давление при тяжелом миокардите снижено.
Аускультация сердца: ослабление I тона, характерен ритм галопа, который предшествует появлению клинических признаков сердечной недостаточности и служит важным диагностическим признаком миокардита. При развитии легочной гипертензии II тон усилен над легочной артерией, а при полной блокаде левой ножки пучка Гиса может быть расщеплен. У значительной части больных отмечается систолический шум за счет относительной недостаточности митрального и (или) трехстворчатого клапанов. При сопутствующем перикардите определяется шум трения перикарда. В тяжелых случаях отмечаются признаки выраженной застойной бивентрикулярной сердечной недостаточности: набухание шейных вен, альтернирующий пульс, резко выраженная кардиомегалия, застойные хрипы в легких и выпот в плевральные полости, увеличение печени, анасарка.
Дополнительные методы исследования:
ЭКГ:
· Уплощенные, двухфазные или отрицательные зубцы Т, депрессия сегмента ST. В тяжелых случаях регистрируются глубокие «коронарные зубцы Т и патологические зубцы Q и QS, что часто затрудняет дифференциальную диагностику с инфарктом миокарда;
· Частыми находками являются нарушения проводимости. Особенно характерна блокада левой ножки пучка Гиса (20%) и предсердно-желудочковые блокады, включая полную с приступами Морганьи-Адамса-Стокса;
· Среди нарушений ритма наиболее часто встречаются желудочковая экстрасистолия, пароксизмальная желудочковая тахикардия.
Рентгенография грудной клетки
· У значительной части больных изменения отсутствуют. В тяжелых случаях отмечается разной степени выраженности кардиомегалия, признаки венозного застоя в легких;
· При сопутствующем экссудативном перикардите сердце приобретает шаровидную форму.
Эхокардиография
· Дисфункция левого желудочка (ЛЖ);
· Нормальный или увеличенный размер камеры ЛЖ;
· Сегментарные нарушения подвижности стенки;
· Пристеночные тромбы в полостях сердца, чаще в ЛЖ.
Катетеризация сердца
· Повышенное конечно-диастолическое давление в ЛЖ;
· Сегментарные нарушения подвижности стенки;
· Рестриктивный тип гемодинамики в начальных стадиях заболевания.
Радиоизотопные методы
Томосцинтиграфия миокарда с цитратом галлия-(Gа-67). При этом методе галлий захватывается нейтрофильными лейкоцитами и активированными Т-лимфоцитами, которые мигрируют в очаг воспаления и накапливаются там. С этой же целью используются антимиозиновые антитела, меченные индием-111 (In111). Специфичность сцинтиграфии с Gа-67 составляет 100%, а чувствительность достигает 85%.
http://infopedia.su/5x4c76.html
Далласские критерии миокардита
Согласно классическим критериям Dallas, при диагностике миокардита необходимо провести гистологическое исследование для достоверности диагноза. Однако из-за низкой чувствительности гистологического метода, обусловленной неоднородным характером воспалительного инфильтрата в миокарде, а также из-за нежелания клиницистов прибегать к инвазивной процедуре, миокардит во многих случаях остается недиагностированным.
В связи с тем что доля этого заболевания, вероятно, значительно больше, чем оценивают, для верификации диагноза необходимы высокая степень клинического подозрения помимо клинических и лабораторных критериев, а также использование новых возможностей визуализации, чтобы не прибегать без необходимости к биопсии.
В соответствии с новыми диагностическими стратегиями заподозрить миокардит можно при наличии двух категорий, а расценить как высоко вероятный — в случае, если есть три категории и более: (1) соответствующие клинические симптомы; (2) доказательство изменений структуры или функции сердца либо повреждение миокарда при отсутствии регионарной коронарной ишемии; (3) локальное отсроченное контрастное усиление или повышение Т2-сигнала на КМРТ; (4) наличие воспалительного инфильтрата или обнаружение вирусного генома при анализе результатов биопсии миокарда либо по данным лабораторных исследований. Конечно, биопсия миокарда до сих пор позволяет провести наиболее специфичную диагностику миокардита.
Например, миокардит должен быть заподозрен, когда у молодого пациента необъяснимые симптомы СН или боли в груди, но на ангиограмме определяются нормальные КА. Когда молодой пациент с минимальными ФР в отношении патологии КА жалуется на острую боль в груди или на ЭКГ есть ишемические отклонения, в 32% случаев продолжают поиск подтверждений острого миокардита с помощью биопсии согласно критериям Dallas, а еще у большего количества пациентов будет выявлен вирус-позитивный геном при молекулярном анализе. Главным ограничением точной диагностики миокардита является недостаток неинвазивных высокочувствительных и специфических инструментов, которые можно было бы широко использовать.
Наиболее обсуждаемые методы диагностики и их предполагаемая чувствительность и специфичность перечислены в таблице ниже.
а) Клинические симптомы. Клинические симптомы миокардита не являются специфическими и в большой степени зависят от проявлений заболевания. Молодые пациенты чаще всего предъявляют жалобы на боль в груди и усталость. У пациентов с нарушенной функцией сердца могут наблюдаться впервые появившаяся СН, одышка или усталость. У некоторых больных могут быть симптомы наджелудочковых или желудочковых аритмий, включая ощущение сердцебиения, пресинкопальные состояния и синкопе. В наиболее тяжелых случаях, например при молниеносном миокардите, у пациентов могут наблюдаться кардиогенный шок и неустраняемые аритмии.
У некоторых больных могут быть конституциональные нарушения, например лихорадка и продромальные явления. Однако данные проявления редки и полагаться на них при диагностике нельзя.
б) Лабораторные и инструментальные исследования. Тяжелый миокардит может приводить к вторичным повреждениям миокарда, обусловленным наличием воспалительного инфильтрата и активации цитокинов помимо прямого поражения клеток вирусом. Эти процессы могут серьезно снизить функцию сердца и стать причиной его повреждения, что можно определить по утечке таких сердечных ферментов, как креатинкиназа (КК) или тропонин, если повреждение серьезное или хроническое. Однако в большинстве случаев утечка ферментов относительно мала, а стандартные лабораторные методы исследования КК и ее фракции МВ (КК-МВ) практически нечувствительны (общая чувствительность составляет только 8%).
Такие биомаркеры, как тропонин, более полезны, когда используют высокочувствительные пороговые величины. Например, когда в качестве границы используют пороговую величину тропонина Т (ТрТ) в сыворотке выше 0,1 нг/мл, чувствительность повышается с 34 до 53% без влияния на специфичность. Сходные наблюдения были отмечены и для тропонина I (ТрI). Другие биомаркеры (цитокины, компоненты системы комплемента, антивирусные или антикардиальные антитела) либо слишком нечувствительны, либо неадекватно стандартизированы для того, чтобы использовать их в общей клинической практике.
Повреждение сердца также может проявиться нарушениями на ЭКГ, которые могут варьировать от инверсии зубца Т до выраженного подъема сегмента ST и АВ-блокад в зависимости от области и распространенности воспалительного повреждения. В серии исследований, проведенных Kuhl и соавт., было отмечено, что аритмии (как наджелудочковые, так и желудочковые) могут наблюдаться у 55% пациентов.
Методы визуализации, например двухмерная ЭхоКГ, могут быть полезны для начальной оценки состояния пациента с целью определения локальной дисфункции желудочков, которая часто сопровождает данное заболевание. Признаки ремоделирования желудочков, включая расширение полостей сердца, регионарную гипертрофию, а также локальные нарушения сократимости стенки, при миокардите наблюдаются нередко, но данные изменения можно не отличить от изменений при ишемии миокарда или ИМ.
Отсутствие регионарного заболевания КА и быстрое восстановление функции желудочков при последующем наблюдении являются общими подсказками в диагностике миокардита. Ретроспективный анализ ЭхоКГ 42 пациентов с миокардитом, подтвержденным результатами биопсии, обнаружил дисфункцию желудочков у 69% пациентов, но наличие дилатации сердца варьировало в больших пределах. Такие новые технологии, как УЗИ тканей и тканевая допплерография, имеют большую диагностическую ценность. Для окончательного диагноза необходимы дополнительные оценочные исследования.
ЭхоКГ, безусловно, является полезным методом последующего наблюдения с целью мониторирования естественной динамики функции желудочков или ответа организма пациента на лечение. Двухмерная ЭхоКГ может помочь отличить молниеносный миокардит от классического: в последнем случае наблюдается меньшее пространственное диастолическое увеличение, но увеличивается толщина перегородки, а также наблюдается значительно более выраженная дилатация желудочков.
Визуализация с помощью антимиозиновых антител, меченных индием-111, позволяет определить миоциты, утратившие целостность клеточной мембраны. Эти антитела связываются с внутриклеточным миозином при наличии иммунного или вирусного повреждения. Визуализация с помощью индия-111 имеет хорошую чувствительность (83%), но низкую специфичность (53%) в отношении миокардита.
Сочетание положительного результата визуализации с помощью антимиозиновых антител с нежелудочковой дилатацией является предиктором высокой частоты положительных результатов биопсии миокарда и может быть использовано как неинвазивный диагностический метод первой ступени.
в) Кардиальная магнитно-резонансная томография. Визуализация с помощью КМРТ является новым подходом в диагностике миокардита. Этот метод визуализации привлекателен тем, что позволяет определить миокардит по характеристикам ткани в зависимости от содержания в ней воды и изменений кинетики контрастного вещества. КМРТ также позволяет визуализировать весь миокард, поэтому подходит для определения локальной неоднородной природы повреждений миокарда. Местный воспалительный процесс при миокардите приводит к выбросу цитокинов и мобилизации воспалительных клеток в пораженные участки, что, в свою очередь, обусловливает локальные изменения в проницаемости мембран, отек ткани и в конечном счете фиброз.
Эти изменения напрямую влияют на параметры Т2-релаксации тканей, зависящие от содержания в них воды. Более того, такие внеклеточные контрастные вещества, как гадолиний диэтилентриаминпентаацетат (ДТПА), также по-разному распространяются и выводятся в воспаленной и рубцовой тканях по сравнению со здоровой тканью, что ведет к изменениям при Т1-релаксации и, соответственно, изменениям контрастирования или к о тсроченному контрастному усилению на Т1-взвешенных изображениях.
Оценка точности определения миокардита с помощью КМРТ показала относительное преимущество Т2-взвешенных изображений, включая инверсию последовательности восстановления. Этот подход к определению повреждений при миокардите имеет чувствительность 84% и специфичность 74%, установленные на основании результатов биопсии или доказательств естественного течения миокардита.
Использование Т2-взвешенных изображений помимо Т1-взвешенных изображений с гадолинием ДТПА и локального отсроченного контрастного усиления в дальнейшем увеличило диагностическую точность метода до 90% и более при сравнении всех текущих исследований. Феномен отсроченного контрастного усиления часто ассоциируется с недавним некрозом сердечной ткани или излеченным ИМ, но в случае миокардита этот феномен можно использовать для дальнейшего увеличения чувствительности и специфичности диагностики. Механизм данного явления еще не ясен, возможно, он связан с отложением локальных коллагеновых пучков во время процесса заживления, которые могут временно связываться с гадолинием ДТПА и таким образом задерживать его выведение.
Возможность определения с помощью КМРТ с контрастным усилением локализации ткани с характерными аномалиями одновременно с визуализацией регионарной подвижности стенки позволила выбирать нужный участок для биопсии (КМРТ-направленная биопсия). Mahrholt и соавт. использовали этот метод биопсии миокарда у 32 пациентов с подозрением на миокардит. Биопсия из аномальных участков выявила положительные (71%) и отрицательные (100%) предрасполагающие факторы. Метод КМРТ-направленной биопсии показал, что именно боковая стенка является наиболее типичным местом развития поражения, а не перегородка, откуда обычно берут образцы материала для биопсии.
КМРТ из-за относительной ее неинвазивности можно проводить повторно для контроля естественного течения заболевания и мониторирования ответа организма на терапию.
г) Биопсия миокарда. Гистологическое исследование. Критерии Dallas при диагностике миокардита представляли собой первую попытку стандартизировать патологическую сторону заболевания. По критериям Dallas необходимо наличие воспалительного инфильтрата и ассоциированного некроза миоцитов или повреждения, нехарактерного для ишемического события. При пограничном миокардите должен присутствовать менее интенсивный воспалительный инфильтрат, а микроскопические признаки деструкции миоцитов — отсутствовать. Несмотря на нечувствительность критериев Dallas при диагностике миокардита, они остаются «золотым стандартом» для постановки однозначного диагноза.
Существует множество причин нечувствительности критериев Dallas. Из-за неоднородной природы повреждений миокарда при стандартной биопсии миокарда с забором образца миокардиальной ткани массой 30 мг срабатывает принцип «пан или пропал». Chow и McManus впервые показали данную нечувствительность на посмертной биопсии сердца пациентов с миокардитом: при единичной эндомиокардиальной биопсии гистологически выявить миокардит удалось лишь в 25% случаев. Даже в случае 5 биопсий поставить правильный диагноз «миокардит» по классическим критериям Dallas смогли лишь в 70% случаев.
Использование в дальнейшем МРТ позволило объяснить эту нечувствительность: оказывается, ранние воспалительные процессы в миокарде локализовались в основном на боковой стенке ЛЖ (труднодоступное место для стандартного биотома). Таким образом, при проведении стандартной эндомиокардиальной биопсии существует значительная вероятность ошибки в диагностике миокардита. Для урегулирования ситуации появились варианты интерпретации гистологических образцов, подготовленные экспертами-патологами. Например, из 111 пациентов, включенных в исследование Myocarditis Treatment Trial, спонсированное National Institutes of Health (NIH), с диагнозом «миокардит» по результатам биопсии сердца, только у 64% диагноз был подтвержден после изучения тех же образцов биопсии экспертной группой патологов.
В текущем руководстве АСС/АНА по лечению СН эндомиокардиальную биопсию расценивают как рекомендацию класса IIb. Биопсию миокарда обычно выполняют пациентам с быстро прогрессирующей КМП, рефрактерной к традиционным методам лечения, или с необъяснимой КМП, связанной с прогрессирующим заболеванием проводящей системы сердца либо жизнеугрожающими желудочковыми аритмиями. Также стоит рассмотреть необходимость биопсии при наличии признаков и симптомов ССЗ у пациентов с системным заболеванием, которое вызывает дисфункцию ЛЖ. Биопсию в плановом порядке всем пациентам с подозрением на миокардит не проводят.
1. Риски эндомиокардиальной биопсии. По результатам исследований уровень осложнений при биопсии миокарда у пациентов с ДКМП составляет 2-5%. Приблизительно 50% осложнений связаны с венозным доступом (непреднамеренная пункция артерии, пневмоторакс, вазовагальная реакция или кровотечение после удаления), а остальные — с самой процедурой. Использование УЗИ для определения внутренней яремной вены и/или катетеризации вены повышает вероятность успеха, а также уменьшает уровень осложнений и время доступа. Осложнениями, связанными с процедурой, могут быть аритмии, нарушения проведения и перфорация сердца, которая способна привести к тампонаде перикарда, а иногда и к смерти.
Пациенты с перфорацией жалуются на боль, которой во время процедуры в норме быть не должно. Состояние таких пациентов может быстро ухудшиться вследствие кровоизлияния в полость перикарда и дисфункции ЛЖ. Накопление крови в перикардиальном пространстве может привести к формированию тромба, что может помешать чрескожной перикардиальной эвакуации крови. Пациентам, которых не удается немедленно реанимировать посредством чрескожного перикардиоцентеза, проводят открытую эвакуацию крови, для чего нужны координация с сердечно-сосудистыми хирургами и подготовленная операционная на случай редких, но возможных осложнений. Уровень осложнений при проведении биопсии через бедренную вену практически равен уровню при проведении процедуры через яремную вену. Выполнение биопсии ЛЖ имеет сходный риск перфорации, несмотря на большую толщину стенки ЛЖ.
2. Молекулярное исследование. Традиционные критерии Dallas, основанные на патологоанатомическом анализе биопсии миокарда, имеют определенные ограничения, а преимущества молекулярных технологий в определении вирусного генома и воспалительной активации в материале одного и того же биоптата в значительной мере расширили возможности по выявлению вирусного миокардита, вирусной этиологии, а также повысили чувствительность биопсии как диагностического метода.
Методы определения вирусного генома, например гибридизация in situ, направленная на поиск вирусного генетического материала в патологических образцах, и множественная амплификация с помощью ПЦР образцов РНК, увеличили чувствительность и показали, что вирусная РНК в значительной степени ассоциируется с симптомами и прогнозом. Однако удивительно, что наличие вирусного генома абсолютно не связано с наличием или отсутствием воспалительных клеток в материале одной и той же биопсии. Таким образом, биоптат может быть положительным только по критериям Dallas, положительным только по молекулярным показателям, положительным в обоих случаях или полностью отрицательным. Это свидетельствует о том, что миокардит является либо заболеванием с молекулярным триггером в виде вируса, либо иммунным ответом организма-хозяина.
Анализ иммунологической активации в образцах биопсии может дать дополнительную информацию. Можно изучить материал и определить подтипы клеток в воспалительном инфильтрате или сигнальной активации, например сигналы цитокинов или компонентов системы комплемента. Образцы также помогут определить регуляцию антигенов главного комплекса гистосовместимости. Чувствительность и специфичность регуляции антигенов главного комплекса гистосовместимости по исследованиям образца малых размеров были на уровне 80 и 85% соответственно, но это не было подтверждено при изучении больших образцов. Тем не менее в одном исследовании, оценивавшем иммуносупрессивную терапию, экспрессию главного комплекса гистосовместимости использовали для выбора терапии пациентам с миокардитом и воспалительной КМП.

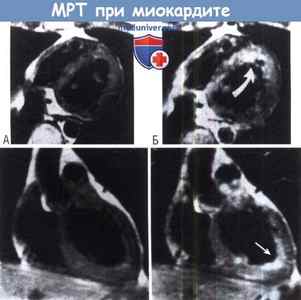
(А) Т1-взвешенная трансаксиальная (вверху) и венечная (внизу) МРТ левого желудочка пациента с миокардитом перед контрастированием.
(Б) МРТ после контрастирования на тех же уровнях после инъекции контрастного вещества.
Отмечено усиление миокардиального сигнала с перегородки и области верхушки (стрелки).
http://dommedika.com/cardiology/diagnostika_miokardita.html
Диагностические критерии миокардита 1 страница
К большим критериям отнесены — перенесенная инфекция и появление в течение 10 дней после нее:
• застойной сердечной недостаточности,
• полной AV-блокады с синдромом Морганьи — Адамса — Стокса,
• патологических изменений ЭКГ,
• повышения активности миокардиальных ферментов в сыворотке
крови.
К малым критериям отнесены:
• лабораторные подтверждения перенесенного вирусного заболева
ния (положительные реакции нейтрализации, РТГАи РСК),
• ослабление I тона,
•ритм галопа,
• результаты субэндомиокардиальной биопсии.
Для диагностики легкого течения миокардита достаточно наличия в анамнезе предшествующей инфекции и сочетания двух больших критериев или одного из них с двумя малыми. Наличие же в числе крите-
Некоронарогенные болезни сердца одного из трех первых позволяет констатировать среднетяжелое
или тяжелое течение миокардита.
Изменения сегмента ST(смещение вверх или вниз) и зубца 7ушю-щение, двухфазность или инверсия) на ЭКГ могут быть самыми ранними, а нередко и единственными проявлениями поражения миокарда при инфекционных заболеваниях. Одним из признаков миокардита часто служит относительная тахикардия, не соответствующая температуре тела. Нарушения возбудимости и проводимости во время инфекционного заболевания всегда свидетельствуют о присоединившемся миокардите. Для миокардита типичными являются расстройства предсердно-желудочковой и внутрижелудочковой проводимости (блокады ножекпучка Гиса, различные степени AV-блокады) и разнообразные нарушения ритма (политопная желудочковая или суправен-трикулярная экстрасистолия, фибрилляция предсердий).
Иногда различного вида аритмии являются единственным признаком текущего миокардита. Приводим клинический пример.
Больной Г., 57лет, госпитализирован в клинику Института кардиологии 04.06.97г. с жалобами на общую слабость, ощущение дискомфорта в области сердца, одышку при незначительной физической нагрузке (ходьба на несколько метров), выраженные отеки нижних конечностей, вынужденное положение в постели (невозможностьлечь), боль в правом подреберье. Состояние резко ухудшилось в апреле 1997 г., когда появились выраженная одышка в покое, усиливающаяся при малейшей физической нагрузке, ощущение перебоев в работе сердца, отеки нижних конечностей. Незадолго до этого больной перенес острую респираторную инфекцию.
При поступлении в клинику состояние тяжелое: диффузный цианоз кожи и слизистых оболочек, пульсация шейных вен, массивные отеки нижних конечностей. Выраженная одышка в покое, усиливающаяся при перемене положения тела, частота дыхания 28 в 1 мин, положение ортопноэ. Пульс 80— 84 в 1 мин, неритмичный, частые экстрасистолы. Тоны приглушены, I тон меняющейся интенсивности, иногда усиленный — «пушечный» тон, грубый систолический шум над верхушкой. Показатели анализа крови не изменены.
При рентгенографии органов грудной полости с кардиометрией опре-деляется «бычье» сердце, расширено влево за счет гипертрофии левого
169
Некоронарогенные болезни сердца
желудочка, артериальный конус выбухает. Пищевод не отклонен, дуга аорты уплотнена.
На ЭКГ полная атриовентрикулярная диссоциация с правожелудоч-ковой экстрасистолической аритмией на фоне полной блокады правой ножки пучка Гиса. Частота сокращений предсердий (зубцы Р) 86—90 в 1 мин, желудочков — 40 в 1 мин. Патологический зубец Q в отведениях III u aVF, отсутствие увеличения зубца R в грудных отведениях (рис. 14).
Приэхокардиографии в В-режиме обнаружено увеличение размеров правого желудочка с признаками легочной гипертензии, увеличение диаметра левого предсердия (до 48мм). Конечно-систолический объем левого желудочка составил 88 мл, конечно-диастолический —239 мл, ударный — 152 мл, фракция выброса левого желудочка составила 63%за счет объемной перегрузки левого желудочка. Отмечено увеличение правых полостей сердца. Обнаружен частичный надрыв хорд передней створки митрального клапана со свободным про-лабированием части последней в полость левого предсердия. Придопплер-эхо-кардиографическом исследовании диагностирована регургитация на митральном и трехстворчатом клапанах.
Время возникновения полной AV-блокадыустановить неудалось, поэтому проводили дифференциальную диагностику острого инфаркта миокарда, хронической ИБС, дилатационной кардиомиопатии и воспалительного поражения миокарда как наиболее частых причин развития аритмий такого типа.
Диагноз: острый миокардит неуточненной этиологии, тяжелое течение, полная AV-блокада, желудочковая экстрасистолическая аритмия (бигеминия), полная блокада правой ножки пучка Гиса, недостаточность митрального и трехстворчатого клапанов, сердечная недостаточность И Б стадии. В НИИ сердечно-сосудистой хирургии рекомендована имплантация искусственного водителя ритма.
Лечение: глюкокортикоиды—дексаметазон (8мг/сут) внутривенно и пред-низолон (40мг/сут); каптоприл (12,5мг Зраза в сутки), ацетилсалициловая кислота (325мг/сут), мочегонные средства (фуросемид до 6Омг/сут) в зависимости от состояния водного баланса, изосорбид динитрат (ЗОмг/сут).
Состояние больного в течение 2 нед постепенно улучшалось, уменьшилась выраженность симптомов сердечной недостаточности. На ЭКГ: снижение
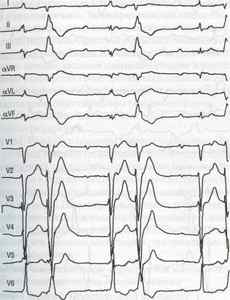
Рис.14. ЭКГ больного при поступлении
степени AV-блокады — неполная AV-блокада типа Мобитц И. 19.06.97г. восстановился синусовый ритм с частотой сердечных сокращений 72 в 1 мин (рис. 15). Значительно улучшилось клиническое состояние пациента, практически исчезли одышка и периферические отеки.
Приведенное наблюдение свидетельствует, что миокардит у больных среднего возраста может протекать нетипично, иногда нарушения ритма сердца и проводимости являются единственными клиническими призна-
171
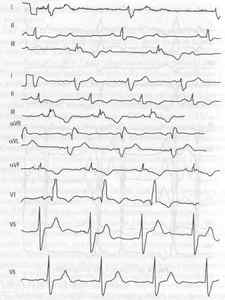
Рис. 15. Динамика ЭКГ больного на фоне лечения
ками воспалительного процесса в миокарде. Всестороннее обследование и аргументированная дифференциальная диагностика позволяют установить правильный диагноз, выбрать адекватную тактику лечения, избежать хирургического лечения, улучшить прогноз заболевания.
772
Некоронарогенные болезни сердца
Данные лабораторных исследований в диагностике миокардита неспе-цифичны и противоречивы. Такие признаки, как лейкоцитоз, увеличение СОЭ и содержания сиаловых кислот, а также температуры тела в качестве критериев собственно миокардита не учитывают, поскольку они могут быть отнесены к иному заболеванию. В последние годы применяются новые диагностические методы, включая иммунологические и вирусологические. Обнаружение в сыворотке крови противокардиалъных антител служит серьезным доводом в пользу диагноза миокардита, однако эти изменения обнаруживаются преимущественно при тяжелых его формах.
Субэндокардиальная биопсия дает много ложноотрицательных и сомнительных результатов.
В 1958 г. М. Weinberg и соавторы впервые осуществили биопсию миокарда у 5 больных во время торакотомии. В 1960 году P. Suton и соавторы внедрили методику чрескожной пункционной биопсии миокарда. В последующие годы в ряде клиник был накоплен достаточно большой опыт применения эндомиокардиальной биопсии, подтвердивший его относительную безопасность. Дискутировался вопрос о количестве участков миокарда, необходимых для суждения о распространенности его поражения.
В 1984 г. был разработан рабочий стандарт — так называемые Далласские критерии диагноза миокардита, предложенные группой американских морфологов.
Далласские диагностические критерии для миокардита по результатам эндомиокардиальной биопсии Первичная биопсияОпределенный миокардит
Пограничный (вероятный) миокардит Отсутствие миокардита
Повторные биопсииПродолжающийся (персистирующий) миокардит Разрешающийся (заживающий) миокардит Разрешившийся (заживший) миокардит
Строгим диагностическим критерием острого миокардита признается наличие воспалительной клеточной инфильтрации миокарда с некрозом и/или дегенерацией кардиомиоцитов, нетипичной для ише-мического повреждения. Термин «пограничный миокардит» исполь-
173
Некоронарогенные болезни сердца
зуется в случаях выявления клеточной инфильтрации и неповрежденных кардиомиоцитов. Данные повторных биопсий позволяют определить динамику или исход процесса и говорить о персистирующем разрешающемся или разрешившемся процессе.
В1998 г Всемирной федерацией сердца был принят Консенсус по определению воспалительной кардиомиопатии (миокардита) по докладам двух экспертных комитетов. Острый миокардит рассматривается как активный миокардит, хронический — как пограничный или заживающий миокардит.
При первичной биопсии можно диагностировать:
1. Острый (активный) миокардит: наличие инфильтрата (диффуз
ного или локального) с определением не менее 14 инфильтрирующих
лимфоцитов на 1 мм 2 (это количество должно включать преимуществен
но Т-лимфоциты (CD45ro) или активированные Т-клетки и до 4 мак
рофагов). Количественно инфильтрат должен быть подсчитан имму
ногистохимическим методом. Определяется некроз или дегенерация,
должен учитываться также фиброз, наличие которого не обязательно.
2. Хронический миокардит: наличие инфильтрата, содержащего не
менее 14 инфильтрирующих лимфоцитов на 1 мм 2 (это количество
должно включать преимущественно Т-лимфоциты (CD45ro) или ак
тивированные Т-клетки и до 4 макрофагов). Количественно инфильт
рат должен быть подсчитан иммуногистохимическим методом. Некроз
и дегенерация обычно не выражены, должен учитываться фиброз.
3. Отсутствие миокардита: не обнаруживаются инфильтрирующие
клетки или их количество менее 14 на 1 мм 2 .
Для оценки фиброза разработаны критерии: отсутствие фиброза — 0-я степень, начальный фиброз — 1-я степень, умеренный фиброз — 2-я степень, выраженный фиброз — 3-я степень.
При последующих биопсиях можно диагностировать:
1. Продолжающийся (персистирующий) миокардит: критерии 1 или 2.
2. Разрешающийся (заживающий) миокардит: критерии 1 или 2, но
иммунологический процесс более вялый, чем при первичной биопсии.
3. Разрешившийся (заживший) миокардит. Соответствует Даллас
ской классификации. Всем категориям может сопутствовать или не
сопутствовать фиброз.
Г74
Некоронарогенные болезни сердца
При хроническом миокардите субэндокардиальная биопсия не по-оляет выявить патогномоничные признаки уже через 1-2 мес от на-
заболевания после проведения адекватной терапии. В последнее время эндомиокардиальная биопсия применяется огра-иченно — метод технически сложен. Некоторые авторы высказывали пасения по поводу метода, в сомнительных случаях рассеянные интер-стициальные клетки могут располагаться между миоцитами и быть приняты за настоящие лимфоциты, при очаговом миокардите может быть случайно захвачена интактная ткань. Считается, что лишь у ограниченного числа больных с клинически подозреваемым миокардитом диагноз может быть однозначно верифицирован с помощью биопсии сердца. Несмотря на то, что эндомиокардиальная биопсия является диагностическим стандартом при остром миокардите, низкая частота его выявления отражает неспособность диагностировать заболевание только с помощью гистологических критериев, применяемых в настоящее время.
Следовательно, все инструментальные и лабораторные методы исследования позволяют подтвердить наличие миокардита, однако отрицательные результаты не являются критерием исключения диагноза.
С помощью посевов крови и других биологических жидкостей можно подтвердить вирусную этиологию миокардита. На недавно перенесенную вирусную инфекцию указывает четырехкратное повышение титра противовирусного IgG в период выздоровления по сравнению с острым периодом. Методами диагностики вирусной инфекции могут также быть метод культивирования вируса, реакция полимеризации цепей вирусной ДНК, выявление антигенов.
При миокардите с большей, чем при другой патологии сердца, частотой выявляются антитела к миозину, актину, миолемме. К. Schulze и соавторы (1989) считают обнаружение аутоантител к адениннуклеотид-ному транслокатору— ферменту внутренней мембраны митохондрий — органоспецифичным для миокардита.
В последнее время достигнуты значительные успехи в идентификации Давно известных сывороточных маркеров повреждения миоцитов: повышение сывороточного тропонина I, который регулирует кальцийопосредо-
175
Некоронарогенные болезни сердца
ванное взаимодействие актина и миозина, является чувствительным и высокоспецифичным сывороточным маркером повреждения сердца. Поскольку большая часть сердечного тропонина I физически связана с сократительным аппаратом миоцита, после повреждения сердца он медленно выделяется в сьгеоротку, где может обнаруживаться в сроки до 14 дней. Это обеспечивает более широкое диагностическое поле для определения повреждения сердца, чем, например, МВ-фракция креатинфосфокиназы.
В настоящее время для установления диагноза миокардита перспективным представляется использование сцинтиграфии с галлием-67 — радиоизотопом, тропным к зонам воспаления, с технеция пирофосфа-том, а также сцинтиграфии с моноклональными антителами к миозину, меченными индием-111.
Выявление изменений в тканях, обусловленных миокардитом, возможно с помощью магнитно-резонансной томографии.
Достоверный диагноз миокардита установить очень трудно, так как миокардит может быть совершенно бессимптомным или проявляться различными неспецифическими симптомами. Даже отрицательные результаты биопсии не исключают диагноз миокардита. В острой фазе миокардита активность сердечных изоферментов обычно повышена, что может повлечь ошибочный диагноз инфаркта миокарда. Диагноз миокардита почти всегда является в определенной степени предположительным, но становится весьма убедительным, если к нему присоединяются признаки сопутствующего перикардита.
Дифференциальный диагноз.Следует дифференцировать миокардит и НЦЦ, миокардиодистрофию, ИБС, первичный ревмокардит, тиреотоксикоз, перикардит, дилатационную кардиомиопатию.
При ревматизме значительно меньше «кардиальных» жалоб, особенно на боль в области сердца, но характерным являются артралгия и артрит. При миокардите чаще наблюдается астенизация. При ревматизме изолированный миокардит — явление исключительное, часто в процесс вовлекается эндокард и формируются пороки сердца. Миокардит неревматического генеза, как правило, является изолированным. Для ревматического поражения характерна склонность к рецидивирова-нию, миокардит рецидивирует редко.
Некоронарогенные болезни сердца
Тиреотоксикоз напоминает миокардит в тех случаях, когда в клинической картине на первый план выступают изменения сердца, а другие симптомы, характерные для тиреотоксикоза, появляются позже. Доминируют жалобы больных на ощущение нехватки воздуха, сердцебиение, нарушение ритма сердца. Боль в области сердца чаще отмечается при миокардите, тогда как раздражительность, уменьшение массы тела, потливость, мелкий тремор — при поражении щитовидной железы. Тахикардия при тиреотоксикозе не поддается противовоспалительной терапии, но эффективно применение антитиреоидных препаратов. Исследование функции щитовидной железы радиоактивным йодом, сканирование щитовидной железы, определение в крови содержания тиреоидных гормонов помогает верифицировать диагноз.
Дифференциальный диагноз миокардита и НЦД описан в разделе функциональных поражений сердца.
Необходимость дифференциальной диагностики миокардитаи ИБС возникает преимущественно при нетипичном для последней болевом синдроме с патологическими изменениями ЭКГ или при наличии только патологических изменений ЭКГ без болевого синдрома. Основные критерии дифференциальной диагностики представлены в табл. 12.
Наиболее сложна дифференциальная диагностика тяжелого миокардита с дилатационной кардиомиопатией. Ряд исследователей считают последнюю следствием диффузного миокардита, в частности вызванного вирусом Коксаки. По клиническим проявлениям эти заболевания достаточно близки. В пользу кардиомиопатии свидетельствует постепенное развитие признаков застойной сердечной недостаточности без проявлений аллергии и сенсибилизации, изменений гематологических показателей воспаления. Отсутствует положительная динамика признаков застойной сердечной недостаточности, показателей ЭКГ и эхокардиограммы под влиянием противовоспалительного лечения.
Прогноз. Вбольшинстве случаев (до 90%) миокардит протекает бес-
имптомно и в течение 1 — 2 мес заканчивается полным выздоровлением,
исчезаютвсе субъективные симптомы, нормализуется ЭКГв покое и при
Проведении велоэргометрии. У многих больных сохраняются остаточные
измнения ЭКГ, указывающие на развитие очагового миокардитического
Некоронарогенные болезни сердца
Таблица 12. Основные критерии дифференциального диагноза миокардита и ИБС